题目内容
16.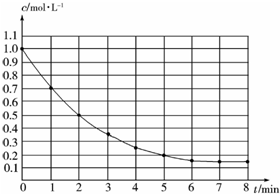 如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )
如图表示反应X(g)?4Y(g)+Z(g)△H<0,在某温度时X的浓度随时间变化的曲线,下列有关该反应的描述正确的是( )| A. | X的平衡转化率为85% | |
| B. | 第6 min 后,反应就终止了 | |
| C. | 若升高温度,X的平衡转化率将大于85% | |
| D. | 若降低温度,v正减小,v逆增大 |
分析 A、依据图象分析x的变化浓度,结合化学反应速率概念计算分析;
B、反应达到平衡是动态平衡,反应没有停止;
C、反应是放热反应,升温,平衡向吸热反应方向进行;
D、降温正逆反应速率减小,但反应有能量变化,平衡一定发生移动.
解答 解:A、x的平衡转化率=$\frac{1.0mol/L-0.15mol/L}{1.0mol/L}$×100%=85%,故A正确;
B、反应达到平衡是动态平衡,正逆反应速率相同,反应仍然进行,故B错误;
C、反应是放热反应,升温,平衡向吸热反应方向进行,x的平衡转化率将小于85%,故C错误;
D、反应是放热反应,若降低温度,反应正向进行,v正和v逆减小,减少的程度不同,故D错误;
故选A.
点评 本题考查化学平衡影响因素方向判断,掌握化学平衡移动原理是解题关键,题目难度中等.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案
相关题目
6.下列电离方程式正确的是( )
| A. | CaCl2=Ca2++Cl2- | B. | Ba(NO3)2=Ba+2+2NO3- | ||
| C. | NaHSO4=Na++H++SO42- | D. | NaHCO3=Na++H++CO32- |
7.下列物质属于电解质的是( )
| A. | NH3 | B. | SO3 | C. | 盐酸 | D. | H2SO4 |
4.CuBr2分解的热化学方程式为:2CuBr2(s)=2CuBr(s)+Br2(g)△H=+105.4kJ/mol
在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa.
如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为( )
在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa.
如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为( )
| A. | p(Br2)≤4.66×103Pa | B. | 2.33×103Pa<p(Br2)≤4.66×103Pa | ||
| C. | <p(Br2)>2.33×103Pa | D. | 2.33×103Pa≤p(Br2)≤4.66×103Pa |
11.下列变化中必须加入适当的氧化剂才能实现的是( )
| A. | MnO2→Mn2+ | B. | PCl3→PCl5 | C. | HCl→H2 | D. | H2O2→O2 |
8.A、B、C、D为短周期元素,且原子序数依次增大.已知A原子的最外层电子数是其电子层数的2倍,B是地壳中含量最高的元素,B原子的最外层电子数是D原子最外层电子数的2倍,C原子最外层只有一个电子.下列说法正确的是( )
| A. | 非金属性:A>B | |
| B. | 四种元素中,C处于元素周期表中最左、下方,故原子半径最大 | |
| C. | 元素B和C只能形成一种化合物 | |
| D. | A、C、D的最高价氧化物对应的水化物中没有两性氢氧化物 |
6.锆(Zr)元素是核反应堆燃料棒的包裹材料,二氧化锆(ZrO2)可以制造耐高温纳米陶瓷.我国有丰富的锆英石(ZrSiO4)含Al2O3、SiO2、Fe2O3等杂质,碱熔法生产锆的流程如下:
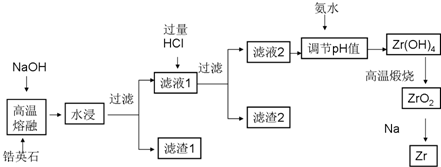
已知25℃时部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
(1)完成高温熔融时的主要反应方程式:
ZrSiO4+4NaOH=Na2ZrO3+Na2SiO3+2H2O
(2)为了提高浸出率可采取的方法有将原料粉碎增大接触面积、加热或搅拌或多次浸取(列举两种)
(3)生成滤渣2的成分H2SiO3 或 H4SiO4(用化学式表示)
(4)用氨水将滤液2的pH调至2.4≤pH<3.4,目的是使Zr4+完全转化为Zr(OH)4沉淀,同时保证Al3+不会被沉淀下来.
(5)往流程中滤渣1中加入盐酸溶液,过滤不溶物后,再将滤液在不断通入HCl气流中气流同时蒸发结晶,可回收得到铁的氯化物FeCl3晶体.

已知25℃时部分阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 | Zr(OH)4 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀时pH | 1.2 | 2.7 | 3.4 | 6.3 |
| 完全沉淀时pH | 2.4 | 3.2 | 5.2 | 9.7 |
ZrSiO4+4NaOH=Na2ZrO3+Na2SiO3+2H2O
(2)为了提高浸出率可采取的方法有将原料粉碎增大接触面积、加热或搅拌或多次浸取(列举两种)
(3)生成滤渣2的成分H2SiO3 或 H4SiO4(用化学式表示)
(4)用氨水将滤液2的pH调至2.4≤pH<3.4,目的是使Zr4+完全转化为Zr(OH)4沉淀,同时保证Al3+不会被沉淀下来.
(5)往流程中滤渣1中加入盐酸溶液,过滤不溶物后,再将滤液在不断通入HCl气流中气流同时蒸发结晶,可回收得到铁的氯化物FeCl3晶体.
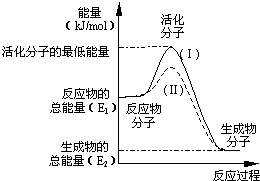 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察下图,然后回答问题:
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察下图,然后回答问题: .
.