��Ŀ����
8��ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̣���ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ��
C��s��+H2O��g��?CO��g��+H2��g����H=+131.3kJ•mol-1����S=+133.7J•��K•mol�� -1
�ٸ÷�Ӧ�ܷ��Է��������¶��йأ�
��һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����bc ������ĸ����ͬ��
a�������е�ѹǿ���� b��1mol H-H�����ѵ�ͬʱ����2molH-O��
c��U����CO��=U����H2O�� d��c��CO��=c��H2��
���� �ٸ��ݡ�G=��H-T��S�жϣ���G��0����Ӧ�Է����У�
�ڸ��ݻ�ѧƽ��״̬��������𣬵���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯������ʱҪע�⣬ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
��� �⣺�����Ȼ�ѧ��Ӧ����ʽ��֪����ӦΪ�������������̣�����H��0����S��0����G=��H-T��S��0��Ӧ�Է����У����Ը÷�Ӧ�Է����У����¶�Ӱ�죬298��ʱ����H=+131.3kJ•mol-1��S=+133.7J•mol-1•K-1����G=��H-T��S=+131.3kJ•mol-1-��298+273��K����+133.7��10-3KJ•mol-1��•K-1=54.96KJ/mol��0��˵����Ӧ���Է����У�
�ʴ�Ϊ���¶ȣ�
��a��һ���¶��£���һ���ݻ��ɱ���ܱ������з���������Ӧ����Ӧǰ����������ʵ��������仯���淴Ӧ������������ʵ������ӣ�ѹǿ�����ֺ�ѹ�������е�ѹǿʼ�ղ��䣬����˵����Ӧ����ƽ�⣬��a����
b��1 molH-H�����ѵ�ͬʱ����2mol H-O��������2mol H-O��ͬʱ����l molH-H����˵����Ӧ����ƽ�⣬��b��ȷ��
c����Ӧ����֮�ȵ��ڻ�ѧ����ʽ������֮�ȣ�v����CO��=v����H2O����˵��ˮ������Ӧ���ʺ��淴Ӧ������ͬ����Ӧ�ﵽƽ��״̬����c��ȷ��
d�����ݷ�Ӧ��֪����ʼ����c��CO��=c��H2��������˵����Ӧ����ƽ�⣬��d����
��ѡ��bc��
���� ���⿼�黯ѧƽ��״̬�жϼ���Ӧ���Է���Ϊ��Ƶ���㣬����Ӱ�����ؼ�ƽ������Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���

| A�� | Ԫ�����ڱ���7�������8������ | B�� | ��A���Ԫ��ȫ���Ƿǽ���Ԫ�� | ||
| C�� | Ԫ�����ڱ���7������ | D�� | ������ָ��1��2���� |
| A�� | �����ܽ�Ȳ�ͬ�����ýᾧ�� | B�� | ֱ�Ӽ��ȷ� | ||
| C�� | �����ռ� | D�� | ����AgNO3��Һ |
| A�� | ���������ȱ�ɰ�ɫ��ĩ | B�� | �������������������ֽ� | ||
| C�� | �ɱ����� | D�� | ��ʯ����ˮ��Ӧ������ʯ�� |
| A�� | ����0.9mol | B�� | ����0.9mol����1.8mol | ||
| C�� | ����1.8mol | D�� | ��0.9mol |
| A�� | 1.8��10-7mol•L-1 | B�� | 1.0��10-5 mol•L-1 | ||
| C�� | 1.0��10-7 mol•L-1 | D�� | 1.8��10-9 mol•L-1 |
| A�� | �Ȼ�����Һ�ڵ��������µ���������Ӻ������� | |
| B�� | ��ˮ��Һ�������Ϊ�����ƶ������ӵĻ������ǵ���� | |
| C�� | CO2��ˮ��Һ����������������CO2��������� | |
| D�� | ��ǿ����ʵ�ˮ��Һ��ֻ������û�з��� |
| ������ | ���������� | ���������� | �� | �� | �� |
| A | CO | CuO | H2SO4 | NH3•H2O | Na2S |
| B | CO2 | Na2O | HCl | NaOH | NaCl |
| C | SO2 | Na2O2 | CH3COOH | KOH | CaF2 |
| D | NO2 | CaO | HNO3 | Cu��OH��2CO3 | CaCO3 |
| A�� | A | B�� | B | C�� | C |
| A�� | ������̼������Һ��Ӧ��2H++CO32-=CO2��+H2O | |
| B�� | ��ȩ����������Cu��OH��2��Һ��Ӧ��HCHO+2Cu��OH��2$\stackrel{��}{��}$HCOOH+Cu2O��+2H2O | |
| C�� | ʵ������Һ��ͱ��ڴ������������屽��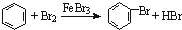 | |
| D�� | ��CO2ͨ�뱽������Һ��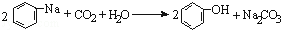 |