题目内容
6.下列化学方程式或离子方程式正确的是( )| A. | 乙酸与碳酸钠溶液反应:2H++CO32-=CO2↑+H2O | |
| B. | 甲醛与足量新制Cu(OH)2浊液反应:HCHO+2Cu(OH)2$\stackrel{△}{→}$HCOOH+Cu2O↓+2H2O | |
| C. | 实验室用液溴和苯在催化剂作用下制溴苯: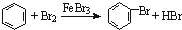 | |
| D. | 将CO2通入苯酚钠溶液: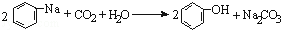 |
分析 A.乙酸为弱酸,离子方程式中乙酸不能拆开;
B.1mol甲醛完全反应生成2mol氧化亚铜,该反应不满足电子守恒;
C.苯与液溴在催化剂存在条件下能够发生取代反应生成溴苯;
D.苯酚的羧酸大于碳酸氢钠,苯酚钠与二氧化碳在溶液中反应生成苯酚和碳酸氢钠.
解答 解:A.CH3COOH为弱酸,在离子方程式中应写成化学式,其正确的离子方程式为:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO-,故A错误;
B.甲醛与足量新制Cu(OH)2浊液反应的离子反应为:HCHO+4Cu(OH)2$\stackrel{△}{→}$H2CO3+2Cu2O↓+4H2O,故B错误;
C.实验室用液溴和苯在催化剂作用下制溴苯的化学反应为: ,故C正确;
,故C正确;
D.碳酸的酸性比苯酚的酸性强,所以苯酚钠通入二氧化碳生成苯酚和碳酸氢钠,正确的化学方程式为:C6H5ONa+CO2+H2O→C6H6OH+NaHCO3,故D错误;
故选C.
点评 本题考查离子反应方程式及化学反应方程式书写的正误判断,为高频考点,题目难度中等,把握发生的反应及离子反应的书写方法为解答的关键,试题侧重有机反应的考查.

练习册系列答案
相关题目
9.百服宁口服液为解热镇痛药,主要用于治疗头痛、发烧.其主要化学成分的结构简式为:
下列有关该有机物叙述正确的是( )

下列有关该有机物叙述正确的是( )
| A. | 分子式为C8H10NO2 | |
| B. | 该有机物是苯酚的同系物 | |
| C. | 其属于α-氨基酸的同分异构体有3种 | |
| D. | 该有机物可与FeCl3溶液发生显色反应 |
6.分子式为C5H10Cl2的有机分子中,所含有的甲基数不可能为( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
1.用氮化硅(Si3N4)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的热效率.工业上用化学气相沉积法制备氮化硅的反应如下:3SiCl4(g)+2N2(g)+6H2(g)$\frac{\underline{\;高温\;}}{\;}$Si3N4(s)+12HCl(g)△H<0,一定温度下,恒容密闭容器中进行该反应,下列措施能增大正反应的反应速率的是( )
| A. | 分离出少量氮化硅 | B. | 降低温度 | ||
| C. | 充入氮气 | D. | 充入氦 |
18.对一个有气体参与的反应,下列能加快反应速率且不改变活化分子百分数的是( )
| A. | 定容容器中通入惰性气体 | B. | 增大压强 | ||
| C. | 升温 | D. | 加入催化剂 |
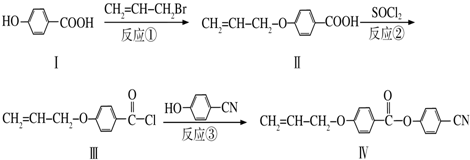
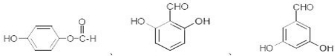 任一种.
任一种.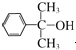 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是 .
. ,(2)H2O2:
,(2)H2O2: ,
, ,(4)CO2:
,(4)CO2: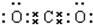 .
.