题目内容
固体X只可能由A1、(NH4)2SO4 ,MgCl2.FeCl2, AlCl3, AgN03中的一种或几种组成,某同学对该固体进行了如下实验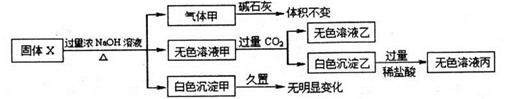
下列判断正确的是:
| A.气体甲一定是纯挣物 |
| B.白色沉淀甲可能是混合物 |
| C.固体X中一定存在AlCl3、(NH4)2SO4, MgCl2 |
| D.固体X中一定不存在FeCl2、AgNO3 |
D
解析试题分析:铝和硫酸铵与过量浓氢氧化钠溶液生成氢气和氨气,氢气和氨气均不能被碱石灰吸收,A错误;氯化镁、氯化亚铁、硝酸银能与过量氢氧化钠溶液生成氢氧化镁、氢氧化亚铁、氢氧化银三种白色沉淀,但氢氧化亚铁能被氧气氧化生成红褐色氢氧化铁、氢氧化银能分解生成棕色氧化银,所以白色沉淀甲只能是氢氧化镁,B错误、D正确;氯化铝与过量氢氧化钠溶液生成偏铝酸钠,二氧化碳与偏铝酸钠溶液生成氢氧化铝白色沉淀,氢氧化铝溶于盐酸,所以固体X中肯定有氯化铝,铝和硫酸铵至少有一种,C错误。
考点:元素及其化合物

练习册系列答案
相关题目
下列叙述正确的是
| A.CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| B.铜片加入氯化铁溶液中发生反应:3Cu+2Fe3+=3Cu2++2Fe |
| C.FeCl2、Fe(OH)3、Cu2S均可通过化合反应制得 |
| D.在pH=1溶液中,NH4+、K+、ClO-、Cl-可以大量共存 |
下列有关实验现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 把SO2通入紫色石蕊试液中 | 紫色褪去 | SO2具有漂白性 |
| B | 把浓硫酸滴到pH试纸上 | 试纸变红 | 浓硫酸具有酸性 |
| C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变浅 | 反应2NO2 N2O4的△H<0 N2O4的△H<0 |
| D | 向AgCl沉淀中滴加KI溶液 | 白色沉淀变为黄色 | 溶度积:AgI比AgCl更小 |
用4种溶液进行实验,下表中“试剂和操作”与“现象”对应关系正确的是
| 选项 | 试剂和操作 | 现象 |
| A | 向AlCl3溶液中滴入过量的氨水 | 溶液先有白色沉淀,后来沉淀消失 |
| B | 向新生成的AgC1浊液中滴入KI溶液,振荡 | 白色沉淀逐渐转化为黄色沉淀 |
| C | 向Ca(C1O)2溶液中先通入CO2,再加入少量品红溶液 | 溶液先变浑浊,通入CO2后品红的红色不褪去 |
| D | 向BaC12溶液中先通入SO2,再通入过量NO2 | 先生成沉淀,后来沉淀消失 |
向100mL18mol/L的硫酸中加入足量铜片,加热并充分反应。下列有关说法正确的是
| A.充分反应后转移1.8mol电子 | B.H2SO4只作氧化剂 |
| C.若不加热应生成H2 | D.消耗的铜的质量一定少于57.6g |


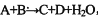 ;请回答下列问题:
;请回答下列问题: