题目内容
下列叙述正确的是
| A.CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| B.铜片加入氯化铁溶液中发生反应:3Cu+2Fe3+=3Cu2++2Fe |
| C.FeCl2、Fe(OH)3、Cu2S均可通过化合反应制得 |
| D.在pH=1溶液中,NH4+、K+、ClO-、Cl-可以大量共存 |
C
解析试题分析:A、CO2、SO2都是酸性氧化物,与水反应生成相应的含氧酸。NO2与水反应生成硝酸和NO,属于氧化还原反应,原理不同,A不正确;B、铜的金属性弱于铁的,与氯化铁反应生成氯化亚铁和氯化铜,反应的离子方程式是Cu+2Fe3+=Cu2++2Fe2+,B不正确;C、FeCl2、Fe(OH)3、Cu2S均可通过化合反应制得,有关反应的方程式分别是Fe+2FeCl3=3FeCl2、4Fe(OH)2+O2+2H2O=4Fe(OH)3、2Cu+S Cu2S,C正确;D、pH=1的溶液显酸性,ClO-不能大量共存,D不正确,答案选C。
Cu2S,C正确;D、pH=1的溶液显酸性,ClO-不能大量共存,D不正确,答案选C。
考点:考查CO2、SO2、NO2、铜的性质;物质的制备原理以及离子共存的正误判断等

练习册系列答案
相关题目
下列关于元素及其化合物的说法正确的是
| A.Fe在常温下可与浓硝酸、稀硝酸、浓硫酸剧烈反应 |
| B.Na久置于空气中,可以和空气中的有关物质发生反应,最终生成NaHCO3 |
| C.S、Cl2均能和NaOH溶液发生氧化还原反应,且都既作氧化剂又作还原剂 |
| D.因为碳酸、氨水能够导电,所以液氨、二氧化碳是电解质 |
下列叙述正确的是
| A.NaHCO3固体中既含有离子键,又含有共价键,溶于水后的电离方程式为 NaHCO3=Na++H++CO32- |
B.符合a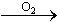 b b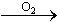 c转化关系的单质a可以是N2、Al、Si、S c转化关系的单质a可以是N2、Al、Si、S |
| C.室温下,pH=3的溶液中,Na+、Fe2+、NO3-、AlO2-四种离子不能大量共存 |
| D.用焰色反应或澄清石灰水均可鉴别Na2CO3与KHCO3溶液 |
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 淀粉溶液中加稀硫酸,加热片刻,滴加银氨溶液,再水浴加热 | 无银镜生成 | 淀粉未发生水解 |
| B | 向溶液X中加入稀盐酸,并将产生的无色气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中一定含有CO32-或HCO3- |
| C | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
| D | 取久置的绿矾(FeSO4·7H2O)溶于水,加入KSCN溶液 | 溶液变为血红色 | 绿矾部分或全部被氧化 |
下列图示与对应叙述相符合的是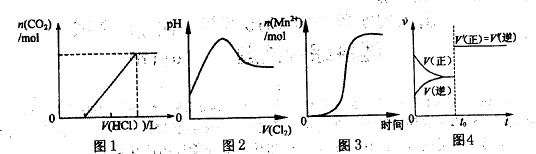
A.图1表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol 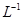 盐酸至过量时,产生气体的体积与消耗盐酸的关系 盐酸至过量时,产生气体的体积与消耗盐酸的关系 |
| B.图2表示C12通入H2S溶液中pH的变化 |
C.图3表示10mL0.01mol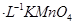 酸性溶液氧化0.1mol 酸性溶液氧化0.1mol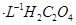 溶液时, 溶液时,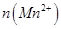 随时间的变化(M 随时间的变化(M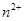 对该反应有催化作用) 对该反应有催化作用) |
D.图4表示已达平衡某反应,在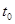 时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |
下列实验和结论不正确的是
| A.明矾和漂白粉均可用于自来水的杀菌、消毒 |
| B.用丁达尔实验可以将Al(OH)3胶体和NaCl溶液区分 |
| C.向KI溶液滴加氯水和CCl4振荡,静置后分层且下层显紫色,则氧化性:Cl2>I2 |
| D.Al(OH)3与稀H2SO4、NaOH溶液均能反应,说明AI(OH)3是两性氢氧化物 |
固体X只可能由A1、(NH4)2SO4 ,MgCl2.FeCl2, AlCl3, AgN03中的一种或几种组成,某同学对该固体进行了如下实验
下列判断正确的是:
| A.气体甲一定是纯挣物 |
| B.白色沉淀甲可能是混合物 |
| C.固体X中一定存在AlCl3、(NH4)2SO4, MgCl2 |
| D.固体X中一定不存在FeCl2、AgNO3 |