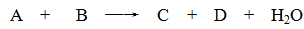题目内容
(6分)某些化学反应可用表示(未配平): ;请回答下列问题:
;请回答下列问题:
(1)若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,写出该反应的离子方程式:_________________________________________________。
(2)若A为紫红色金属,D为无色刺激性气体,请写出符合上式的化学方程式:______________________________________________________________。
(3)若C、D均为气体(其中C有颜色)且分子具有相同的原子个数比,则符合上式化学方程式是:_____________________________________________________。
(1)Cl2+2OH-=Cl-+ClO-+H2O
(2)Cu+2H2SO4(浓) Cu SO4+2H2O+SO2↑
Cu SO4+2H2O+SO2↑
(3)C+4HNO3(浓) CO2↑+4NO2↑+2H2O
CO2↑+4NO2↑+2H2O
解析试题分析:(1) 若A、C、D均含有氯元素,且A中氯元素的化合价介于C与D之间,则该反应是歧化反应,可联想到氯气和碱的反应。
(2)若A为紫红色金属,,可想到A是铜单质,且D为无色刺激性气体,可想到是铜和浓硫酸的反应。
(3)若C、D均为气体(其中C有颜色),且分子具有相同的原子个数比,可想到非金属的反应,即碳与浓硝酸的反应。
考点:符合一定条件的反应。

练习册系列答案
相关题目
固体X只可能由A1、(NH4)2SO4 ,MgCl2.FeCl2, AlCl3, AgN03中的一种或几种组成,某同学对该固体进行了如下实验
下列判断正确的是:
| A.气体甲一定是纯挣物 |
| B.白色沉淀甲可能是混合物 |
| C.固体X中一定存在AlCl3、(NH4)2SO4, MgCl2 |
| D.固体X中一定不存在FeCl2、AgNO3 |
有关元素X、Y、Z、D、E的信息如下:
| | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074 nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102 nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物可溶于水,且能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为___________。
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)_______。
①保存EY2溶液时,需向溶液中加入少量E单质
②EY2只能通过置换反应生成,EY3只能通过化合反应生成
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
(3)将Z单质在X的单质中燃烧的产物和等物质的量的Y单质同时通入足量的水中,充分反应后的溶液中滴入品红溶液,现象是__________________,有关反应的离子方程式为________________________________________________________________________。
 下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中正确的是
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中正确的是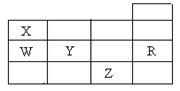
| A.常压下五种元素的单质中,Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物比X的氢化物稳定 |
| D.Y元素最高价氧化物对应水化物比W元素的最高价氧化物对应水化物的酸性强 |