题目内容
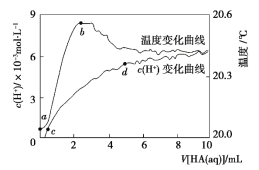
【题目】常温下向 100 mL 蒸馏水中滴入10 mL 5 mol·L-1HA溶液,利用传感器测得溶液中 c (H+)和温度随着加入 HA 溶液体积的变化曲线如图所示,下列有关说法正确的是
A.HA 是强酸
B.a ~ b 段,HA 电离放热,使溶液温度升高
C.c ~ d 段, c (H+)增大,HA 电离程度增大
D.c 点时,加入等体积等浓度的 NaOH 溶液,则 c (Na+)= c (A-)+ c (HA)
【答案】D
【解析】
弱酸存在电离平衡,弱酸的电离吸热,但离子与水结合为水合离子放热,根据物料守恒回答问题。
A. 根据图像可知,随着加入HA的量不断增大,溶液中氢离子浓度增长速率不断减缓,说明HA 是弱酸,A错误;
B. a ~ b 段,HA 电离吸热,但离子与水结合形成水合离子放热,使溶液温度升高,B错误;
C. c ~ d 段, c (H+)增大,HA 电离平衡逆向移动,HA电离程度减小,C错误;
D. c 点时,加入等体积等浓度的 NaOH 溶液,根据物料守恒, c (Na+)= c (A-)+ c (HA),D正确;
答案为D。

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目