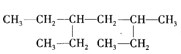题目内容
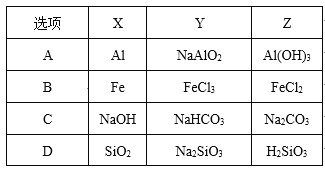
【题目】用酸性![]() 溶液进行下列实验,不能达到预期目的的是( )
溶液进行下列实验,不能达到预期目的的是( )
A.鉴别苯和甲苯
B.鉴别乙烷和乙烯
C.检验![]() 中含碳碳双键
中含碳碳双键
D.鉴别![]() 和
和![]()
【答案】C
【解析】
酸性KMnO4溶液具有强氧化性,可与具有还原性的SO2、亚铁盐等物质发生氧化还原反应,可与甲苯、碳碳双键、醛基等基团发生氧化还原反应,以此解答该题。
A. 甲苯可与酸性高锰酸钾溶液发生氧化还原反应,苯与酸性高锰酸钾不反应,可鉴别,故A正确;
B. 乙烯中碳碳双键可与酸性高锰酸钾溶液发生氧化还原反应,乙烷不与酸性高锰酸钾反应, B正确;
C. CH2=CHCHO中碳碳双键和醛基都可与酸性高锰酸钾溶液发生氧化还原反应,不能检验是否含有碳碳双键,故C错误;
D. SO2具有还原性,可与酸性KMnO4溶液发生氧化还原反应而褪色,![]() 不反应,可鉴别,故D正确。
不反应,可鉴别,故D正确。
答案选C。

 阅读快车系列答案
阅读快车系列答案【题目】铜矾(主要成分 CuSO4·5H2O)是一种可用于食品添加的铜强化剂。现以某硫铁矿渣(含有 CuSO4、CuSO3、Cu2O及少量难溶于酸的Cu2S、CuS)制备铜矾的工艺过程如下:
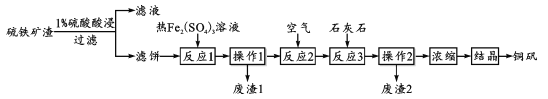
(1)“1%硫酸酸浸”时,固液质量比为1:3并进行4~6次浸取,其目的是_________;
(2)“滤饼”中含有Cu,其中Cu在“反应1”中溶解的离子方程式为________;“废渣1”中只含有S单质,则“反应1”中Cu2S与Fe2(SO4)3反应的物质的量之比为_______。
(3)“反应2”中通入空气的目的是_______;结合离子方程式,说明“反应3”加入石灰石的作用________。
(4)为了提高硫铁矿渣的利用率和产品的产率,在“浓缩”前进行的必要操作是_____;分析下列溶解度信息,最适宜的结晶方式为_________。
t/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 |
CuSO4·5H2O/(g/100g H2O) | 23.1 | 27.5 | 32.0 | 37.8 | 44.6 | 61.8 | 83.8 |
(5)将铜矾、生石灰、水按质量比依次为1.0:0.56:100混合配制无机铜杀菌剂波尔多液,其有效成分为CuSO4·xCu(OH)2·yCa(OH)2。当x=1时,试确定y的值为____。
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
B.增大压强使平衡向生成Z的方向移动
C.在25℃下,反应的平衡常数为1600,改变温度可以改变此反应的平衡常数
D.在25℃下,测得c(X)=0.04mol·L-1,c(Y)=0.1mol·L-1,c(Z)=0.08mol·L-1,则此时v正<v逆