题目内容
【题目】据《科技日报》报道,我国科学家研制成功一系列石墨烯限域的3d过渡金属中心(Mn、Fe、Co、Ni、Cu)催化剂,在室温条件下以H2O2为氧化剂直接将CH4氧化成C的含氧化合物。请回答下列问题:
(1)在Fe、Co、Ni、Cu中,某基态原子核外电子排布遵循“洪特规则特例”(指能量相同的原子轨道在全满、半满、全空状态时,体系的能量最低),该原子的外围电子排布式为__。
(2)在第四周期所有元素中,基态原子未成对电子数最多的元素是__(填元素符号)。
(3)金属晶体热导率随温度升高会降低,其原因是__。
(4)铜的焰色反应呈___。在现代化学中,常用于区分晶体与非晶体的方法为___。
(5)Mn和Co的熔点较高的是___,原因___。
(6)钴晶胞和白铜(铜镍合金)晶胞分别如图1、2所示。

①钴晶胞堆积方式的名称为__;
②已知白铜晶胞的密度为dg·cm-3,NA代表阿伏加德罗常数的值。图2晶胞中两个面心上铜原子最短核间距为__pm(列出计算式)。
【答案】3d104s1 Cr 电子气中的自由电子在热的作用下与金属原子频繁碰撞(温度升高电阻增大) 绿 X-射线衍射法 Co 价电子数多半径小金属键强 六方最密堆积 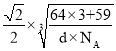 ×1010
×1010
【解析】
(1)在Fe、Co、Ni、Cu中,Cu遵循“洪特规则特例”,3d轨道为全满状态;
(2)在第四周期所有元素中,基态原子最多有6个未成对电子;
(3)金属通过自由电子与金属离子碰撞导热;
(4)x射线衍射法是一种研究晶体结构的方法;
(5)金属键越强,金属晶体的熔点越高;
(6)先根据晶体的密度计算晶胞的边长,再计算两个面心上铜原子最短核间距;
(1)在Fe、Co、Ni、Cu中,Cu遵循“洪特规则特例”,3d轨道为全满状态,Cu原子的外围电子排布式为3d104s1;
(2)在第四周期所有元素中,基态原子未成对电子数最多的原子,外围电子排布式为3d54s1,该元素符号是Cr;
(3)电子气中的自由电子在热的作用下与金属原子碰撞的概率增大,这样电子气不易将动能传远,导热率自然下降;
(4)铜的焰色反应呈绿色。在现代化学中,对固体进行X射线衍射实验区分晶体与非晶体, 所以区分晶体与非晶体的方法为X-射线衍射法;
(5)Mn和Co相比,Co价电子数多、半径小, Co金属键强,所以熔点较高的是Co;
(6)①图1为六方晶胞,所以钴晶胞堆积方式是六方最密堆积;
②设晶胞的边长为a pm,则晶胞的体积为![]() ,根据均摊原则,1个晶胞含有铜原子数是
,根据均摊原则,1个晶胞含有铜原子数是![]() 、镍原子数是
、镍原子数是![]() ,
,![]() ,
,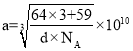 ,晶胞中两个面心上铜原子最短核间距为
,晶胞中两个面心上铜原子最短核间距为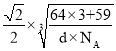 ×1010。
×1010。

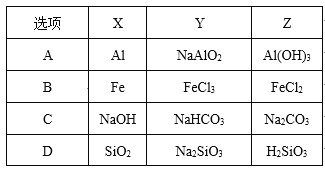
【题目】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是
A.反应达到平衡时,X的转化率为50%
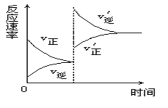
B.增大压强使平衡向生成Z的方向移动
C.在25℃下,反应的平衡常数为1600,改变温度可以改变此反应的平衡常数
D.在25℃下,测得c(X)=0.04mol·L-1,c(Y)=0.1mol·L-1,c(Z)=0.08mol·L-1,则此时v正<v逆
【题目】在相同容积的4个密闭器中进行同一种可逆反应,2A(g)+B(g)![]() 3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
3C(g)+2D(g),起始时4个容器所盛A、B的量如表所示各容器所盛物质的量:
容器 | 甲 | 乙 | 丙 | 丁 |
A | 2mol | 1mol | 2mol | 1mol |
B | 1mol | 1mol | 2mol | 2mol |
在相同温度下,建立平衡时,4个容器中A或B的转化率的大小关系是
A.A的转化率为:甲<丙<乙<丁B.A的转化率为:甲<乙<丙<丁
C.B的转化率为:甲>丙>乙>丁D.B的转化率为:丁>乙>丙>甲