题目内容
3.对可逆反应平衡:A(g)+3B(g)?2C(g)△H<0,下列叙述错误的是( )| A. | 升高温度,v(正)、v(逆)都增大,但v(正)增的更大 | |
| B. | 增大压强,v(正)、v(逆)都增大,但v(正)增的更大 | |
| C. | 增大A的浓度,v(正)会增大,但v(逆)会减小 | |
| D. | 采用适当催化剂(正),v(正)、v(逆)同时增大,而且增大的倍数相同 |
分析 A、升高温度化学反应速率加快,反应向着吸热方向进行;
B、增大压强化学反应速率加快,反应向着气体的系数和减小的方向进行;
C、增大物质的浓度反应速率加快,反应向消耗该物质的方向进行;
D、使用催化剂可同时、同等程度的改变正逆反应速率.
解答 解:A、升高温度v(正)、v(逆)都增大,同时反应向着逆方向进行,v(逆)增的更大,故A错误;
B、增大压强v(正)、v(逆)都增大,同时反应向着正方向进行,v(正)增的更大,故B正确;
C、增大A的浓度v(正)、v(逆)都会增大,同时反应向着正方向进行,v(正)增的更大,故C错误;
D、使用催化剂可同时、同等程度的改变正逆反应速率,所以采用正的催化剂一般v(正)、v(逆)同时增大,而且增大的倍数相同,故D正确.
故选AC.
点评 本题考查学生影响化学反应速率、化学平衡移动的因素知识,注意二者相结合时的灵活应用,难度不大.

练习册系列答案
相关题目
14.进行淀粉水解实验,同时检验水解产物和水解是否完全,除加淀粉和水外,还应加入相应的试剂及加入顺序最好的是( )
| A. | 碘水--过量氢氧化钠溶液--氢氧化铜的悬浊液 | |
| B. | 硫酸溶液--碘水--过量氢氧化钠溶液--氢氧化铜的悬浊液 | |
| C. | 硫酸溶液--过量氢氧化钠溶液--碘水--氢氧化铜的悬浊液 | |
| D. | 硫酸溶液--碘水--氢氧化铜的悬浊液 |
11.O3是重要的氧化剂和水处理剂,在平流层存在:2o3?3O2,2O3?O+O2.粒子X能加速O3的分解:X+O3?XO+O2;XO+O═X+O2(X=Cl、Br、NO等).已知:2O3(g)?3O2(g)△H=-144.8 kJ.mol-1t℃时K=3×1026.下列说法不正确的是( )
| A. | 臭氧层中氟利昂释放出的氯原子是O3分解的催化剂 | |
| B. | 高压放电条件下O2可以转化成O3 | |
| C. | t℃时,3O2(g)?2O3(g),K≈3.33×10-77 | |
| D. | 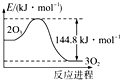 O3转变为O2能量曲线可用图表示 |
18.下列实验方案能达到预期目的是( )
①用蒸馏的方法将海水淡化
②工业上可用金属铝与V2O5在常温下冶炼矾,铝作还原剂
③向溶液中滴入盐酸酸化的氯化钡溶液检验溶液中是否含有SO42-
④向含有Mg(OH)2和Ca(OH)2的浊液中加入足量MgCl2溶液,充分反应后过滤,除去Ca(OH)2.
①用蒸馏的方法将海水淡化
②工业上可用金属铝与V2O5在常温下冶炼矾,铝作还原剂
③向溶液中滴入盐酸酸化的氯化钡溶液检验溶液中是否含有SO42-
④向含有Mg(OH)2和Ca(OH)2的浊液中加入足量MgCl2溶液,充分反应后过滤,除去Ca(OH)2.
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
8.下列实验操作中,正确的是( )
| A. | 稀释浓硫酸时,可先在量筒中加入一定体积蒸馏水,再沿量筒内壁慢慢注入浓硫酸,并用玻璃棒不断搅拌 | |
| B. | 过滤时,玻璃棒的末端应轻轻靠在三层滤纸的一边,漏斗里的溶液应低于滤纸的边缘 | |
| C. | 燃着的酒精灯不慎打翻,应立即用水灭火 | |
| D. | 用药匙或纸槽把粉末状药品送入到试管的底部,如果没有试管夹,可以临时手持试管给固体加热 |
15.镁、铝、铜三种金属粉末混合物,加入过量盐酸充分反应,过滤后向滤液中加入过量烧碱溶液,再过滤,滤液中存在的主要阳离子有( )
| A. | Na+ | B. | Cu2+ | C. | Al3+ | D. | Mg2+ |
12.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 光导纤维的主要成分是二氧化硅,其主要原理是二氧化硅具有较好的导光性 | |
| B. | 盐卤点豆腐、明矾净水与胶体的性质有关 | |
| C. | 新型禽流感病毒H5N1型病毒致死率高,通过高温条件下可杀死H5N1型禽流感病毒 | |
| D. | 雾霾成为现代生活中主要的污染之一,其中PM2.5指标指的是分散质直径在2.5nm的微粒 |
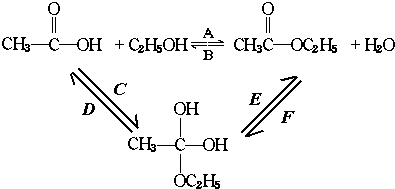
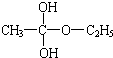 再转化为酯和水,以上反应均为可逆反应,回答下列问题:
再转化为酯和水,以上反应均为可逆反应,回答下列问题: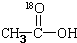 进行该实验,18O可存在于哪些物质中A、C
进行该实验,18O可存在于哪些物质中A、C