题目内容
10.设NA为阿伏加德罗常数的值,下列说法中正确的是( )| A. | 129C60中含有NA个电子 | |
| B. | 46g NO2和N2O4的混合气体含有的原子数为3NA | |
| C. | 标准状况下,22.4L CCl4所含的分子数为6.02×1023 | |
| D. | 100mL0.1mol/LCaCl2溶液中Cl-的物质的量浓度为0.01mol/L |
分析 A、C60由碳原子构成,而1mol碳原子中含6mol电子;
B、NO2和N2O4均由NO2构成;
C、标况下四氯化碳为液体;
D、1mol氯化钙中含2mol氯离子.
解答 解:A、C60由碳原子构成,故129gC60中含有的碳原子的物质的量n=$\frac{129g}{12g/mol}$=10.75mol,而1mol碳原子中含6mol电子,故10.75mol碳原子含有的64.5mol电子即64.5NA个,故A错误;
B、NO2和N2O4均由NO2构成,故46g混合物中含有的NO2的物质的量n=$\frac{46g}{46g/mol}$=1mol,含有3NA个原子,故B正确;
C、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、1mol氯化钙中含2mol氯离子,故0.1mol/L的氯化钙溶液中氯离子的浓度为0.2mol/L,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.取软锰矿石(主要成分为MnO2)116g 跟足量浓盐酸发生如下反应(杂质不参与反应)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,制得22.4L Cl2(标准状况).下列有关说法中不正确的是( )
| A. | 这种软锰矿石中MnO2的质量分数为75% | |
| B. | 被氧化的HCl的物质的量为4mol | |
| C. | 参加反应的HCl的质量为146g | |
| D. | 被还原的MnO2的物质的量为1mol |
1.对于2NaBr+Cl2═2NaCl+Br2反应,下列说法错误的是( )
| A. | 若有16 g Br2生成,则反应过程中转移了0.2 mol电子 | |
| B. | Cl2是氧化剂 | |
| C. | NaBr发生了还原反应 | |
| D. | NaCl为还原产物 |
18.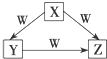 X、Y、Z、W是中学化学常见的四种物质,它们之间具有如图所示转化关系,则下列组合不可能的是:
X、Y、Z、W是中学化学常见的四种物质,它们之间具有如图所示转化关系,则下列组合不可能的是:
( )
 X、Y、Z、W是中学化学常见的四种物质,它们之间具有如图所示转化关系,则下列组合不可能的是:
X、Y、Z、W是中学化学常见的四种物质,它们之间具有如图所示转化关系,则下列组合不可能的是:| X | Y | Z | W | |
| A | NaOH | Na2CO3 | NaHCO3 | CO2 |
| B | O2 | CO2 | CO | C |
| C | AlCl3 | Al(OH)3 | NaAlO2 | NaOH |
| D | S | SO2 | SO3 | O2 |
| A. | A | B. | B | C. | C | D. | D |
15.在150℃时,碳酸铵((NH4)2CO3)加热全部分解成气体得到的气体混合物的密度是相同条件下氢气的( )
| A. | 9倍 | B. | 12倍 | C. | 24倍 | D. | 48倍 |
2.用化学平衡移动的知识分析:25℃时,50mL 0.1mol/L醋酸溶液中,若分别如下改变,对平衡有何影响?(完成表格)
| 改变条件 | 平衡移动方向 | n(H+) | c(H+) | c(CH3COO-) |
| 加入少量的醋酸钠固体 | ||||
| 加入镁条 | ||||
| 加入一定量水稀释 | ||||
| 加入一定量水稀释 | ||||
| 加入浓盐酸 | ||||
| 加入NaOH 固体 |
19.下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.
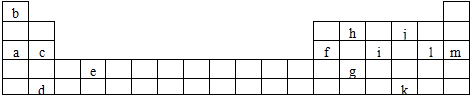
(1)上述元素的单质可能是电的良导体的是a c d e f h(填字母代号).
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ•mol-1):
①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量Li原子失去1个电子后形成稳定结构,再失去1个电子很困难.
②表中Y可能为以上13种元素中的Al(填元素符号)元素.用元素符号表示a和j形成化合物的电子式是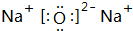 和
和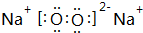 .
.
(3)写出元素e的电子排布式1s22s22p63s23p63d24s2.
(4)以上13种元素中,Ar(填元素符号)元素原子失去核外第一个电子需要的能量最多.
(5)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中,元素c、m分别位于s区、p区.

(1)上述元素的单质可能是电的良导体的是a c d e f h(填字母代号).
(2)下表是一些气态基态原子的第一、二、三、四级电离能(kJ•mol-1):
| 锂 | X | Y | |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | 9550 | 11600 |
②表中Y可能为以上13种元素中的Al(填元素符号)元素.用元素符号表示a和j形成化合物的电子式是
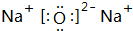 和
和 .
.(3)写出元素e的电子排布式1s22s22p63s23p63d24s2.
(4)以上13种元素中,Ar(填元素符号)元素原子失去核外第一个电子需要的能量最多.
(5)根据元素原子的外围电子排布的特征,可将元素周期表分成几个区域,其中,元素c、m分别位于s区、p区.
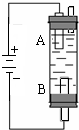 某同学设计了一种电解法制取Fe(OH)2的实验装置(如图).玻璃管内的电解液为NaCl溶液,通电后,溶液中产生白色沉淀,且较长时间不变色.回答下列问题:
某同学设计了一种电解法制取Fe(OH)2的实验装置(如图).玻璃管内的电解液为NaCl溶液,通电后,溶液中产生白色沉淀,且较长时间不变色.回答下列问题: