题目内容
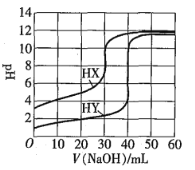
【题目】某化学小组欲测定酸性条件下KClO3溶液与NaHSO3溶液反应的化学反应速率,所用的试剂为10mL 0.1mol/L KClO3溶液和10mL 0.3mol/L NaHSO3溶液,所得c(Cl-)随时间变化的曲线如图所示:

(1)根据实验数据可知,该反应在0~4min的平均反应速率v(Cl-)=______mol/(L·min)。
(2)反应过程中,该反应的化学反应速率变化趋势为先增大后减小。
i.探究化学反应速率增大的影响因素:
已知:ClO3-+3HSO3-=Cl-+3SO42-+3H+
方案 | 假设 | 具体实验操作 |
Ⅰ | 该反应放热,使溶液温度升高,反应速率加快 | 向烧杯中依次加入10mL 0.1mol/L KClO3溶液和10mL 0.3mol/L NaHSO3溶液,______。 |
Ⅱ | 反应产物Cl-对反应有催化作用 | 取10mL 0.1mol/L KClO3溶液于烧杯中,先加入_____固体(填化学式),再加入10mL 0.3mol/L NaHSO3溶液。 |
Ⅲ | 反应中溶液酸性增强,加快了化 学反应速率 | 分别向2个烧杯中加入10mL 0.1mol/L KClO3溶液, 烧杯①:加入1mL水烧杯②:加入1mL 0.2mol/L盐酸再分别向烧杯中加入10mL 0.3mol/L NaHSO3溶液。 |
(问题与思考)
①方案Ⅲ烧杯①中加入1mL水的作用是______。
②在证明方案Ⅰ假设不成立的情况下,从控制变量角度思考,方案III实验操作设计不严谨,改进措施为______。
③除方案Ⅰ、Ⅱ、Ⅲ外,请再提出一个可能使化学反应速率增大的假设_______。
ii.反应后期,化学反应速率降低的主要原因是______。
【答案】2.5×10-3 插入温度计 KCl或者NaCl 空白实验,消除由于体积变化带来的实验影响 将1mL水改为1mL0.2mol/L的KCl溶液(或NaCl溶液) 反应产物SO42-对反应有催化作用(或生成了SO42-加快了化学反应速率) 随着反应进行,反应物浓度降低,反应速率减慢
【解析】
(1)根据v=△c/△t计算;
(2)利用温度计测量溶液温度的变化;根据方案I、Ⅱ所对应的假设的变化分析;根据反应后溶液中的离子成分分析解答;根据氯离子可能会影响反应速率分析;根据浓度对反应速率的影响分析;
(1)根据实验数据可知,该反应在0~4min内生成氯离子的浓度是0.010mol/L,所以平均反应速率v(Cl-)=0.010mol/L÷4min=2.5×10-3mol/(L·min);
(2)①由于是假设该反应放热,使溶液温度升高,反应速率加快,因此需要测量反应过程中溶液温度的变化,则方案I中的实验操作为插入温度计;
②方案I、Ⅱ相比较Ⅱ探究反应产物Cl-对反应有催化作用,所以方案Ⅱ中的应加入Cl-,可加入KCl或者NaCl;
③由于反应中还有硫酸根离子生成,则除I、Ⅱ、Ⅲ中的假设外,还可以提出的假设是生成的硫酸根离子加快了化学反应速率;
④为防止氯离子对实验的干扰,则需要改进的措施是将1mL水改为1mL 0.2mol/L NaCl溶液;
⑤反应后期由于反应物浓度减小,因此化学反应速率变慢。

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案