题目内容
7.美国科学家理查德-海克和日本科学家根岸英一、铃木彰因在研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖.有机合成常用的钯/活性炭催化剂长期使用,催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,需对其再生回收.一种由废钯催化剂制取氯化钯的工艺流程如下:
(1)甲酸在反应中的作用是还原剂(选填:“氧化剂”、“还原剂”).其将PdO转化为钯精渣(Pd)的化学方程式为PdO+HCOOH=Pd+CO2↑+H2O
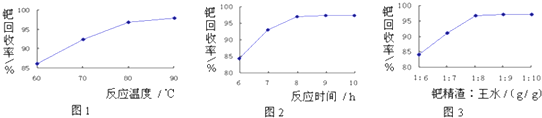
(2)酸溶时钯精渣中钯的回收率高低主要取决于王水溶解的操作条件,已知反应温度、反应时间和王水用量对钯回收率的影响如图1~图3所示,则王水溶解钯精渣的适宜条件为80~90℃(或90℃左右)、反应时间约为8h、钯精渣与王水的质量比为1:8.
(3)王水是浓硝酸与浓盐酸按体积比1:3混合而成的,王水溶解钯的过程中有化合物A和一种无色、能与人体血红蛋白结合而使人中毒气体B生成.
①气体B的分子式:NO;
②经测定,化合物A由3种元素组成,有关元素的质量分数为Pd:42.4%,H:0.8%,则A的化学式为H2PdCl4
(4)加浓氨水时,钯转变为可溶性[P(NH3)4]2+,此时铁的存在形式是Fe(OH)3(写化学式).焙烧2发生反应的化学方程式为Pd(NH3)2Cl2═PdCl2+2NH3↑.
分析 废钯催化剂经烘干后,在700℃的高温下焙烧,C、Fe、Pd、有机物被氧气氧化生成氧化物,向氧化物中加入甲酸,甲酸和氧化铁反应生成盐和水,PdO和甲酸发生氧化还原反应生成Pd,滤渣中含有Pd、SiO2,二氧化硅不溶于王水,但Pd能溶于王水生成溶液,同时生成气体,加入浓氨水调节溶液PH,钯转变为可溶性[Pd(NH3)4]2+,使铁全部沉淀,溶液中加入盐酸酸析得到沉淀,经过脱氨等一系列操作得当氯化钯.
(1)PdO和甲酸发生氧化还原反应生成Pd,Pd的化合价降低,甲酸还原PdO生成Pd、CO2和H2O;
(2)根据Pd回收率与反应温度、反应时间、钯精渣和王水的质量比的关系确定适宜条件;
(3)①王水是浓硝酸与浓盐酸按体积比1:3混合而成的,硝酸具有氧化性,被还原为NO;
②钯在王水中溶解的过程中有化合物A,A中含有的元素为H、Pb、Cl,Cl的百分含量为1-42.4%-0.8%=56.8%;
(4)加浓氨水时,钯转变为可溶性[Pd(NH3)4]2+,碱性溶液中铁离子钡沉淀为氢氧化铁,550℃焙烧2的目的是脱氨.
解答 解:废钯催化剂经烘干后,再在700℃的高温下焙烧,Fe、Pd、有机物被氧气氧化生成氧化物,向氧化物中加入甲酸,甲酸和氧化铁反应生成盐和水,PdO和甲酸发生氧化还原反应生成Pd,滤渣中含有Pd、SiO2,二氧化硅不溶于王水,但Pd能溶于王水生成溶液,同时生成气体,加入浓氨水调节溶液PH沉淀铁离子,得到溶液中中加入盐酸酸析得到沉淀Pd(NH3)2Cl2 ,通过脱氨等一系列操作得当氯化钯.
(1)PdO和甲酸发生氧化还原反应生成Pd,Pb的化合价降低,甲酸作还原剂,PdO和HCOOH发生氧化还原反应生成Pd、CO2和H2O,反应方程式为PdO+HCOOH=Pd+CO2↑+H2O,故答案为:还原剂;PdO+HCOOH=Pd+CO2↑+H2O;
(2)根据图象知,温度越高钯回收率越大,反应时间越长钯回收率越大,钯精渣与王水的质量比越大钯回收率越大,但90℃左右时温度再高钯回收率增大不大;8h后,随着时间的增长,钯回收率增大不大;当钯精渣与王水的质量比为1:8后,再增大钯精渣和王水的质量比,但钯回收率不大,所以适宜条件是80~90℃(或90℃左右)、反应时间约为8 h、钯精渣与王水的质量比为1:8,故答案为:80~90℃(或90℃左右);反应时间约为8h;钯精渣与王水的质量比为1:8;
(3)①王水是浓硝酸与浓盐酸按体积比1:3混合而成的,硝酸具有氧化性,被还原为无色有毒的气体NO,故答案为:NO;
②A中含有的元素为H、Pb、Cl,元素的质量分数分别为Pd:42.4%,H:0.8%,Cl:1-42.4%-0.8%=56.8%,故n(H):n(Pd):n(Cl)=2:1:4,则A的化学式为H2PdCl4,故答案为:H2PdCl4;
(4)加浓氨水时,钯转变为可溶性[Pd(NH3)4]2+,碱性溶液中铁离子钡沉淀为氢氧化铁,脱氨将Pd(NH3)2Cl2变化为PdCl2,发生反应的化学方程式为Pd(NH3)2Cl2═PdCl2+2NH3↑,
故答案为:Fe(OH)3;Pd(NH3)2Cl2═PdCl2+2NH3↑.
点评 本题以Pd的提取为载体考查了工艺流程,涉及化学式的确定、氧化还原反应、图象分析等知识点,明确物质的性质是解本题关键,注意从整体上分析分析解答,知道每一步涉及的反应、物质分离的方法等知识点,结合元素守恒分析解答,题目难度中等.

 习题精选系列答案
习题精选系列答案
| 熔点 | 沸点 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |
(2)若发现C中气泡产生过猛,需要进行的操作的关键是用分液漏斗控制滴加液体的量或滴加速率.
(3)前期P过量生成三氯化磷,后期氯气过量生成五氯化磷,从PCl3和PCl5的混合物中分离出PCl3的最佳方法是a(选填序号).
a.蒸馏 b.分液 c.升华
(4)生成的PCl3在G中收集,则F中盛有冷水,作用是使得三氯化磷液化.
(5)C、D、H所盛的试剂分别是:C饱和食盐水;D浓硫酸;H碱石灰.
(6)如果E中反应放热较多,G处的导管可能发生堵塞,其原因是五氯化磷蒸汽冷却后变成固体.
| A. | 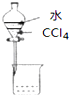 分离水和CCl4 | B. | 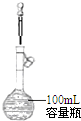 定容 | ||
| C. | 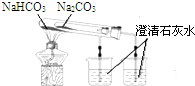 比较两种盐的热稳定性 | D. | 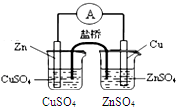 构成铜锌原电池 |
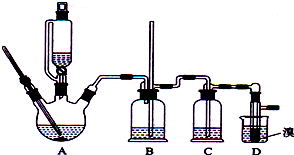 实验室制备1,2-二溴乙烷的反应原理如下:
实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{H_{2}SO_{4}(浓)}$CH2=CH2,CH2=CH2+Br2→BrCH2CHBr
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)实验中制得的1,2-二溴乙烷的产量比理论值低的原因可能是A中反应温度没有迅速升高到170℃,部分乙醇生成了乙醚;A中反应温度过高,乙醇被浓硫酸氧化,生成乙烯的物质的量偏少;A中反应反应速率过快,导致乙烯通入的流速过快反应不充分.(至少写出两种)
(2)判断该制备反应已经结束的最简单方法是溴的颜色完全褪去;
(3)若产物中有少量未反应的Br2,最好用d洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.饱和碳酸钠溶液
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);依据是1,2-二溴乙烷的密度大于水
(5)若产物中有少量副产物乙醚.可用蒸馏的方法除去,理由是1,2-二溴乙烷的沸点132℃大于乙醚的沸点34.6℃,乙醚以气态被分离出去
(6)装置D若使用冰水冷却,则B中的主要现象是玻璃导管中的液面会升高,甚至溢出.
(7)请指出该实验装置的一处不足的地方缺乏尾气处理装置.
| A. | NH4HCO3 | B. | NH4NO3 | C. | (NH4)2SO4 | D. | NH4Br |
 ;
; ;指出分子中化学键是共价键(填‘离子键’或‘共价键’).
;指出分子中化学键是共价键(填‘离子键’或‘共价键’).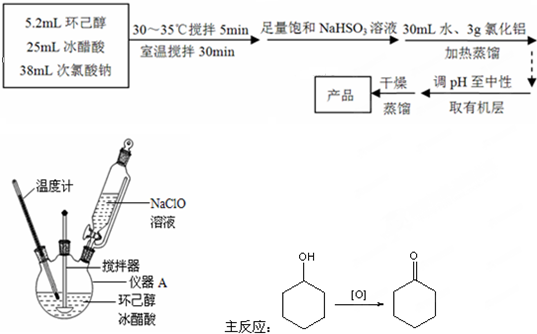
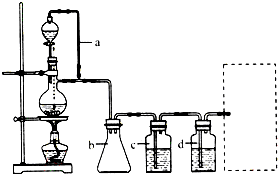 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线: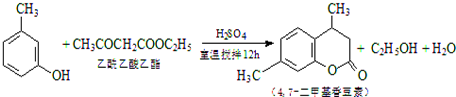
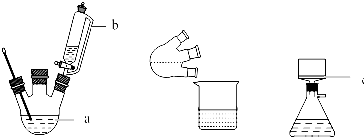
 CH3COOCH2CH3+H2O,用饱和的碳酸钠溶液(填药品名称)收集粗产品,用分液(填操作名称)的方法把粗产品分离.
CH3COOCH2CH3+H2O,用饱和的碳酸钠溶液(填药品名称)收集粗产品,用分液(填操作名称)的方法把粗产品分离.