题目内容
【题目】研究电化学原理与应用有非常重要的意义。
(1)锌锰电池(俗称干电池) 是一种一次电池,生活中应用广泛。
①锌锰电池负极上的电极反应式为:______________________________。
②与普通(酸性)锌锰电池相比较,碱性锌锰电池的优点是____________________(回答一条即可)。
(2)铅蓄电池是最常见的二次电池:Pb+PbO2+2H2SO4 ![]() 2PbSO4+2H2O。
2PbSO4+2H2O。
①充电时阴极反应为:________________________________________。
②用铅蓄电池为电源进行电解饱和食盐水实验(石墨棒为阳极,铁为阴极,食盐水500mL,温度为常温),当电路中有0.05mol电子转移时,食盐水的PH为______(假设溶液体积不变,产物无损耗)。
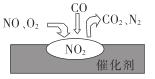
(3)如图是金属(M)-空气电池的工作原理,我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,电池反应为:___________________________ 。二氧化硫—空气质子交换膜燃料电池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。Pt2上的电极反应式为:_______________________________________ 。

(4)高铁酸钠(Na2FeO4)易溶于水,是一种新型多功能水处理剂,可以用电解法制取:Fe+2H2O+2OH![]() FeO42+3H2↑,工作原理如图所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。电解一段时间后,c(OH)降低的区域在_____________(填“阴极室”或“阳极室”);阳极反应为:___________________________。
FeO42+3H2↑,工作原理如图所示。装置通电后,铁电极附近生成紫红色的FeO42,镍电极有气泡产生。电解一段时间后,c(OH)降低的区域在_____________(填“阴极室”或“阳极室”);阳极反应为:___________________________。

【答案】Zn-2e-=Zn2+ 比能量高(或可存储时间长、不易发生电解质的泄漏、或碱性电池使用寿命较长其他合理答案也可) PbSO4+2e-=Pb+SO42- 13 4Al+3O2+6H2O=4Al(OH)3 O2+4H++4e-=2H2O 阳极室 Fe+8OH--6e-=FeO42+4H2O
【解析】
根据原电池、电解池的原理来确定电极,从而进一步推断反应过程。
(1)①锌锰电池中活泼金属锌做负极,失去电子,电极方程式为:Zn-2e-=Zn2+;②普通(酸性)锌锰电池是酸性溶液作电解质,易泄露,相比较碱性锌猛干电池较不稳定,碱性锌锰电池的优点是存储时间长、不易发生电解质的泄漏、或碱性电池使用寿命较长;故答案为:Zn-2e-=Zn2+;存储时间长、不易发生电解质的泄漏、或碱性电池使用寿命较长;
(2) ①铅蓄电池充电时,阴极PbSO4得电子,故阴极反应:PbSO4+2e-=Pb+SO42-;
②电解饱和食盐水过程中,2NaCl + 2H2O![]() 2NaOH + H2 ↑+ Cl2↑,Cl2~2e- ~2OH-,电路中有0.05mol电子转移,即有0.05molOH-生成,可计算出c(OH-)=0.1mol/L,故溶液的pH=13;故答案为:PbSO4+2e-=Pb+SO42-;13;
2NaOH + H2 ↑+ Cl2↑,Cl2~2e- ~2OH-,电路中有0.05mol电子转移,即有0.05molOH-生成,可计算出c(OH-)=0.1mol/L,故溶液的pH=13;故答案为:PbSO4+2e-=Pb+SO42-;13;
(3)根据已知条件,以铝做负极,有空气参与,生成OH-,故方程式为:4Al+3O2+6H2O=4Al(OH)3;燃料电池中Pt1做负极,Pt2做正极得电子,故电极方程式为:O2+4H++4e-=2H2O;
(4)从反应中可知,Fe作阳极,失电子生成FeO42-,故电极方程式为:Fe+8OH--6e-=FeO42-+4H2O,阳极室c(OH-)降低,Ni作阴极,Ni电极消耗H2O生成H2和OH-,电极反应式为2H2O+2e-=H2↑+2OH-,故阴极室c(OH)增大,故答案为:阳极室,Fe+8OH--6e-=FeO42-+4H2O;

【题目】某学生探究0.25mol/LAl2(SO4)3溶液与0.5mol/LNa2CO3溶液的反应,实验如下。
实验1 |
|
实验2 |
|
下列分析正确的是( )
A. 实验1中,白色沉淀a是Al2(CO3)3
B. 实验2中,白色沉淀b一定是Al2(OH)2(CO3)2
C. 检验白色沉淀a、b是否洗涤干净,均可用盐酸酸化的BaCl2溶液
D. 实验1、2中,白色沉淀成分不同的原因与混合后溶液的pH无关