题目内容
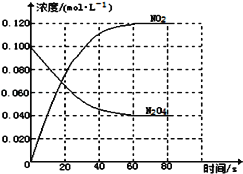
【题目】常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
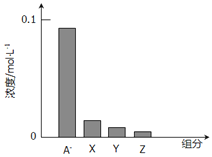
A. HA是强酸
B. 该混合液pH=7
C. 图中x表示HA,Y表示OH-,Z表示H+
D. 该混合溶液中:c(A-)+c(Y)=c(Na+)
【答案】D
【解析】
试题A、0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,得到的溶液为0.1mol/L的NaA溶液,若HA为强酸,则溶液为中性,且c(A-)=0.1mol/L,与图不符,所以HA为弱酸,A错误;B、根据A的分析,可知该溶液的pH>7,错误;C、A-水解使溶液显碱性,所以溶液中的粒子浓度的大小关系是c(Na+)> c(A-)>c(OH-)>c(HA)> c(H+),所以X是OH-,Y是HA,Z表示H+,错误;D、根据元素守恒,有c(A-)+c(HA)=c(Na+),正确,答案选D。

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
【题目】下表是元素周期表的一部分,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为 ________________________ 。
(2)表中能形成两性氢氧化物的元素是 ________ (/span>用元素符号表示),写出该元素的单质与⑨最高价氧化物的水化物反应的离子方程式 ________________________ 。
(3)④元素与⑦元素形成化合物的电子式 _____________________________ 。
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 ____(填化学式)。
(5)③元素与⑩元素两者核电荷数之差是 ____________ 。