题目内容
15.关于元素周期律和周期表,下列说法中正确的是( )| A. | 在周期表中,主族元素的主族序数都等于其原子的最外层电子数 | |
| B. | 周期表中非金属性最强的元素,其最高价氧化物对应水化物的酸性也最强 | |
| C. | 同主族元素随着原子的核电荷数的递增,原子半径依次增大 | |
| D. | 主族元素的单质,随相对分子质量的增大,熔、沸点升高 |
分析 A.主族元素的最外层电子数=主族序数;
B.非金属最强的氟元素,无正价;
C、同主族元素从左到右半径逐渐减小;
D、同主族元素非金属单质的熔沸点从上到下逐渐升高.
解答 解:A.主族元素的最外层电子数=主族序数,如Cl的最外层电子数为7,位于ⅤⅡA族,故A正确;
B.非金属最强的氟元素,无正价,所以也谈不上最高价氧化物对应水化物的酸性了,故B错误;
C、同主族元素从左到右半径逐渐减小,所以同主族元素随着原子的核电荷数的递增,原子半径依次增大,故C正确;
D、同主族非金属元素单质的熔沸点从上到下逐渐升高,ⅠA金属元素的熔沸点从上到下逐渐降低,故D错误;
故选AC.
点评 本题考查学生元素周期律的应用方面的知识,注意知识的归纳和梳理是关键,难度不大.

练习册系列答案
相关题目
5.下列关于乙酸的说法中,正确的是( )
①乙酸易溶于水和乙醇,其水溶液能导电
②无水乙酸又称为冰醋酸,它是纯净物
③乙酸分子里有四个氢原子,所以它不是一元酸
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤1mol乙酸与足量乙醇在浓硫酸作用下可生成88g乙酸乙酯
⑥食醋中含有乙酸,乙酸可由乙醇氧化得到.
①乙酸易溶于水和乙醇,其水溶液能导电
②无水乙酸又称为冰醋酸,它是纯净物
③乙酸分子里有四个氢原子,所以它不是一元酸
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤1mol乙酸与足量乙醇在浓硫酸作用下可生成88g乙酸乙酯
⑥食醋中含有乙酸,乙酸可由乙醇氧化得到.
| A. | ①②③④ | B. | ①②③⑥ | C. | ①②④⑥ | D. | ②④⑤⑥ |
7.下列物质中含有共价键的离子化合物是( )
| A. | Ba(OH)2 | B. | H2O | C. | O2 | D. | CaCl2 |
4.化学与科学、技术、社会、环境密切相关.下列有关说法中错误的是( )
| A. | 节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 | |
| B. | 加热能杀死甲型H1N1流感病毒是因为病毒的蛋白质受热变性 | |
| C. | 太阳能电池板中的硅在元素周期表中处于金属与非金属的交界位置 | |
| D. | 日常生活中的废旧电池会污染环境,所以应集中填埋处理 |
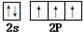 .
.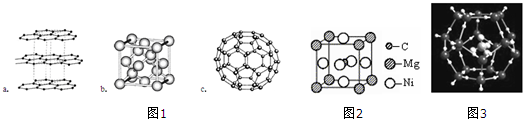
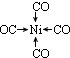 ;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2.
;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2. 、
、 .
.