题目内容
6.(1)硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊如何才能用热水配制出澄清的较浓的CuSO4溶液应加入少量H2SO4;(2)稀Na2S溶液有一种臭鸡蛋气味,加入AlCl3溶液后,臭鸡蛋气味加剧,用离子方程式表示气味加剧过程所发生的反应2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑.
分析 (1)Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,水解呈酸性,可加入酸抑制水解;
(2)Na2S溶液和AlCl3溶液发生互促水解氢氧化铝沉淀和硫化氢气体.
解答 解:(1)因Cu2+水解产生Cu(OH)2,该反应是吸热反应,加热促进水解,故产生浑浊;硫酸浓度增大,平衡逆向移动,能得到澄清的较浓的CuSO4溶液,
故答案为:Cu2+水解产生Cu(OH)2是吸热反应,加热促进水解,故产生浑浊;应加入少量H2SO4;
(2)铝离子能与硫离子发生双水解生成氢氧化铝和硫化氢,反应的离子方程式为:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑,
故答案为:2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑.
点评 本题考查了盐的水解原理应用,题目难度不大,注意把握盐的水解原理及配制能够水解的盐溶液时的方法.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案
相关题目
17.下列反应中,属于取代反应的是( )
| A. | 苯在一定条件下与溴反应生成溴苯 | B. | 乙烯通入溴的四氯化碳溶液 | ||
| C. | 镍催化下苯与氢气反应 | D. | 铜催化下乙醇与氧气反应 |
14.下列物质中既有配位键,又有离子键,还有共价键的是( )
| A. | NH4NO3 | B. | SiO2 | C. | 冰 | D. | O2 |
1.将3.2gCu跟30mL10mol/LHNO3充分反应,还原产物为NO、NO2.若反应后溶液中有amolH+,则此时溶液中含硝酸根离子的物质的量为( )
| A. | 0.5amol | B. | 0.1amol | C. | 0.1+amol | D. | 2amol |
11.有关化学用语正确的( )
| A. | 乙烯的结构式:C2H4 | B. | 四氯化碳的电子式: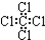 | ||
| C. | 甲烷分子的比例模型: | D. | 苯的分子式: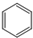 |
18.下列描述不正确的是( )
| A. | 碳原子核外电子有六种运动状态 | B. | NH4+ 中N原子轨道杂化类型为sp3 | ||
| C. | 电负性:O>Cl | D. | 第一电离能 Al>Mg |
15.关于元素周期律和周期表,下列说法中正确的是( )
| A. | 在周期表中,主族元素的主族序数都等于其原子的最外层电子数 | |
| B. | 周期表中非金属性最强的元素,其最高价氧化物对应水化物的酸性也最强 | |
| C. | 同主族元素随着原子的核电荷数的递增,原子半径依次增大 | |
| D. | 主族元素的单质,随相对分子质量的增大,熔、沸点升高 |
16.当酸碱完全中和时( )
| A. | 酸和碱的物质的量一定相等 | |
| B. | 酸能够提供的H+与碱所能提供的OHˉ的物质的量相等 | |
| C. | 酸与碱的质量相等 | |
| D. | 溶液呈中性 |