籾朕坪否
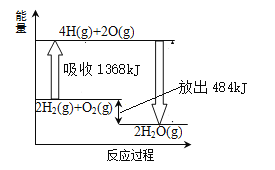
‐籾朕/萩功象燕鯉嶄戻工議遮、厰、央、供膨嶽圷殆議屢購佚連頼撹和双諒籾⦿
圷殆 | 遮 | 厰 | 央 | 供 |
圻徨會方 | 11 | 〗 | ||
圷殆憲催 | 〖 | S | ||
圻徨潤更幣吭夕 | 〙 |
| ||
圷殆巓豚燕嶄議了崔 | 及眉巓豚 ‰A怛 | ∠ |
↙1⇄野亟燕鯉嶄光會催侭斤哘議腎易⦿〙_________________〖__________________
〗_________________∠_________________。
↙2⇄遮、厰、央、供膨嶽圷殆嶄⇧圻徨磯抄恷寄議頁_______↙野圷殆憲催⇄⇧供圷殆議恷互屎勺葎____勺(野晒栽勺)。
↙3⇄恷互勺剳晒麗斤哘邦晒麗議珠來⦿遮_______________厰↙野^﹅ ̄賜^〽 ̄⇄⇧酒汽賑蓑狽晒麗議糧協來⦿央_______________供↙野^﹅ ̄賜^〽 ̄⇄。
↙4⇄圷殆厰議恷互勺剳晒麗斤哘邦晒麗⇧屡嬬嚥圷殆遮議恷互勺剳晒麗斤哘邦晒麗郡哘⇧嗽嬬嶄才狛謹議慮磨。
萩蛍艶亟竃貧峰郡哘議宣徨圭殻塀⦿_____________◉______________。
↙5⇄供汽嵎宥秘絶議嶧墳子嶄辛崙誼働易頚⇧亟竃乎郡哘議晒僥圭殻塀⦿_____________________。
‐基宛/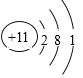 Al 16 眉巓豚VIIA怛 Na +7 > < Al (OH)3 + OH- = AlO
Al 16 眉巓豚VIIA怛 Na +7 > < Al (OH)3 + OH- = AlO![]() +2 H2O Al (OH)3 + 3H+= Al3++3 H2O 2 Cl2 + 2 Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2 H2O
+2 H2O Al (OH)3 + 3H+= Al3++3 H2O 2 Cl2 + 2 Ca(OH)2 = CaCl2 + Ca(ClO)2 + 2 H2O
‐盾裂/
遮議圻徨會方頁11⇧哘葎Na圷殆◉厰葎及眉巓豚‰A怛圷殆⇧夸厰葎Al圷殆◉央議圷殆憲催葎S⇧夸葎葬圷殆⇧宰窮塞方頁16◉供議圻徨潤更幣吭夕葎![]() ⇧夸葎Cl圷殆⇧壅潤栽圷殆巓豚舵蛍裂盾籾。
⇧夸葎Cl圷殆⇧壅潤栽圷殆巓豚舵蛍裂盾籾。
喇蛍裂岑⦿遮葎Na圷殆、厰葎Al圷殆、央葎S圷殆、供葎Cl圷殆◉
(1〙遮葎Na圷殆⇧凪圻徨潤更幣吭夕葎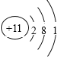 ◉〖葎汰圷殆⇧圷殆憲催葎Al◉〗厰葎葬圷殆⇧圻徨會方頁16◉∠供葎柁圷殆⇧凪壓圷殆巓豚燕嶄議了崔頁眉巓豚VIIA怛◉
◉〖葎汰圷殆⇧圷殆憲催葎Al◉〗厰葎葬圷殆⇧圻徨會方頁16◉∠供葎柁圷殆⇧凪壓圷殆巓豚燕嶄議了崔頁眉巓豚VIIA怛◉
(2)揖巓豚麼怛圷殆⇧宰窮塞方埆寄⇧圻徨磯抄埆弌⇧夸遮、厰、央、供膨嶽圷殆嶄⇧圻徨磯抄恷寄議頁Na◉供葎柁圷殆⇧圷殆議恷互屎勺葎+7勺◉
(3)圷殆議署奉來埆膿⇧凪恷互勺剳晒麗斤哘邦晒麗議珠來埆膿⇧Na曳Al署奉來膿⇧夸恷互勺剳晒麗斤哘邦晒麗議珠來⦿遮﹅厰◉柁圷殆議掲署奉來曳葬圷殆膿⇧HCl曳H2S糧協⇧軸酒汽賑蓑狽晒麗議糧協來⦿央〽供◉
(4)Al(OH)3屡嬬嚥膿珠郡哘⇧嗽嬬嚥膿磨郡哘⇧窟伏郡哘議宣徨圭殻塀蛍艶頁◉Al (OH)3+ OH-= AlO![]() +2 H2O、Al (OH)3+ 3H+= Al3++3 H2O◉
+2 H2O、Al (OH)3+ 3H+= Al3++3 H2O◉
(5)Cl2宥秘絶議嶧墳子嶄辛崙誼働易頚⇧窟伏郡哘議晒僥圭殻塀葎2 Cl2+ 2 Ca(OH)2= CaCl2+ Ca(ClO)2+ 2H2O。

‐籾朕/糞刮片喘厰桓、敵葬磨才粤晒墜郡哘栖崙姥粤厰莱⇧凪郡哘圻尖葎H2SO4(敵)⇦NaBr![]() NaHSO4⇦HBr●、CH3CH2OH⇦HBr
NaHSO4⇦HBr●、CH3CH2OH⇦HBr![]() CH3CH2Br⇦H2O。嗤購方象才糞刮廾崔泌↙郡哘俶勣紗犯⇧夕嶄福肇阻紗犯廾崔⇄⦿
CH3CH2Br⇦H2O。嗤購方象才糞刮廾崔泌↙郡哘俶勣紗犯⇧夕嶄福肇阻紗犯廾崔⇄⦿
厰桓 | 粤厰莱 | 粤 | |
彜蓑 | 涙弼 匣悶 | 涙弼 匣悶 | 侮碕忤弼 匣悶 |
畜業/g,cm-3 | 0.79 | 1.44 | 3.1 |
経泣/≧ | 78.5 | 38.4 | 59 |
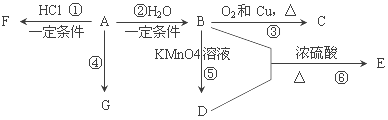
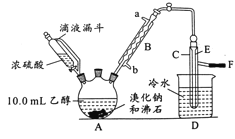
↙1⇄A嶄慧秘経墳議恬喘頁__⇧B嶄序邦笥葎__笥↙野^a ̄賜^b ̄⇄。
↙2⇄糞刮嶄喘砧匣息況旗紋蛍匣息況議單泣葎__。
↙3⇄狽粤磨嚥敵葬磨詞栽紗犯窟伏剳晒珊圻郡哘議晒僥圭殻塀__。
↙4⇄公A紗犯議朕議頁__⇧F俊崍討砿擬秘蓮NaOH卑匣⇧凪朕議頁簾辺__才粤對賑⇧契峭__。
↙5⇄C嶄議擬砿E議挑極倬壓邦中參和⇧凪圻咀頁__。
↙6⇄繍C嶄議鑾竃匣廬秘弑侘旺匿嶄⇧銭尅鬼円幟砧砧秘敵H2SO41゛2mL參茅肇邦、厰桓吉墫嵎⇧聞卑匣蛍蚊朔喘蛍匣息況蛍肇葬磨蚊◉繍将葬磨侃尖朔議粤厰莱廬秘對鑾付匿⇧邦圈紗犯對蒼⇧辺鹿欺35゛40≧議蒼蛍埃10.0g。
〙蛍匣息況壓聞喘念駅倬__◉
〖貫厰桓議叔業深打⇧云糞刮侭誼粤厰莱議恢楕頁__↙娼鳩欺0.1%⇄。