题目内容
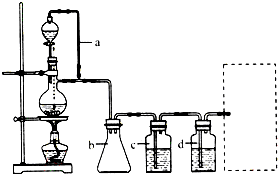
20.TiO2既是制备其他含钛化合物的原料,又是一种性能优异的白色颜料.实验室利用反应TiO2(s)+2CCl4(g)→TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如下: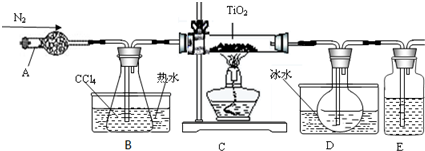
有关性质如下表
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
(2)反应结束前依次进行如下操作:①停止通氮气 ②熄灭酒精灯 ③冷却至室温.正确的顺序为②③①(填序号).
(3)欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(4)使用冰水混合物的目的是冷却TiCl4气体.
(5)TiCl4 遇到湿空气发生强烈的水解,其中一种物质是H2TiO3,试写出该水解反应方程式TiCl4+3H2O═H2TiO3↓+4HCl.
(6)实验室用含量为97%的TiO210克,用上述方法制备TiCl4,最终得到19.8克的产品,则TiO2的转化率为85.95%.
分析 (1)仪器A是干燥管,因为TiCl4遇到水蒸气会水解,所以E中可以用浓硫酸来隔离空气;
(2)对于气体的制取性质实验应该:组装仪器、检验气密性、加装药品,发生反应,终止实验时为防止倒吸,应先熄灭酒精灯,冷却到室温后再停止通入N2;
(3)分离两种沸点不同的液体混合物应该用蒸馏;D中的液态混合物为TiCl4与未反应的CCl4,二者互溶,分离互溶的液体采取蒸馏方法;
(4)使用冰水混合物的目的是冷却TiCl4气体;
(5)盐类水解的实质是结合水电离出的氢离子和氢氧根离子生成弱电解质的过程,TiCl4 遇到湿空气发生强烈的水解,生成H2TiO3、HCl;
(6)根据97%的TiO210克以及TiO2(s)+2CCl4(g)→TiCl4(g)+CO2(g)计算出理论值,转化率=$\frac{实际产量}{理论产量}$.
解答 解:(1)仪器A是干燥管,因为TiCl4遇到水蒸气会水解,所以E中可以用浓硫酸来隔离空气中的水蒸汽,故答案为:干燥管;浓硫酸;
(2)对于气体的制取性质实验应该:组装仪器、检验气密性、加装药品,发生反应,终止实验时为防止倒吸,应先熄灭酒精灯,冷却到室温后再停止通入N2;
故答案为:②③①;
(3)D中的液态混合物为TiCl4与未反应的CCl4,二者互溶,但CCl4和TiCl4是两种沸点差异较大的液体混合物,应该用蒸馏进行分离,故答案为:蒸馏;
(4)在装置C中发生:TiO2(s)+2CCl4(g)→TiCl4(g)+CO2(g),为得到TiCl4,分离二氧化碳,使用冰水混合物将气态的TiCl4冷却,D中的液态混合物为TiCl4与未反应的CCl4,
故答案为:冷却TiCl4气体;
(5)TiCl4与水反应生成氯化氢和二氧化钛的水合物H2TiO3,反应的化学方程式:TiCl4+3H2O═H2TiO3↓+4HCl,故答案为:TiCl4+3H2O═H2TiO3↓+4HCl;
(6)97%的TiO210克,含有n(TiO2)=$\frac{m}{M}$=$\frac{10g×97%}{80g/mol}$=0.12125mol,TiO2(s)+2CCl4(g)→TiCl4(g)+CO2(g),理论产生TiCl4为:0.12125mol×190g/mol=23.0375g,最终得到19.8克的产品,则TiO2的转化率=$\frac{实际产量}{理论产量}$=$\frac{19.8g}{23.0375g}$×100%≈85.95%,故答案为:85.95%.
点评 本题考查实验制备方案,明确原理是解题关键,侧重考查学生装置的分析评价,注意对题目信息的提取与应用,是对学生综合能力的考查,题目难度中等.

| 电离能/kJ•mol-1 | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |

各离子开始沉淀和完全沉淀的pH值
| 离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ | Mg2+ |
| 开始沉淀~沉淀完全的pH | 2.7~4.1 | 3.7~5.2 | 7.5~9.6 | 8.6~10.1 | 9.6~11.1 |
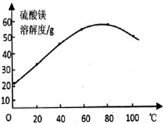
请回答下列问题:
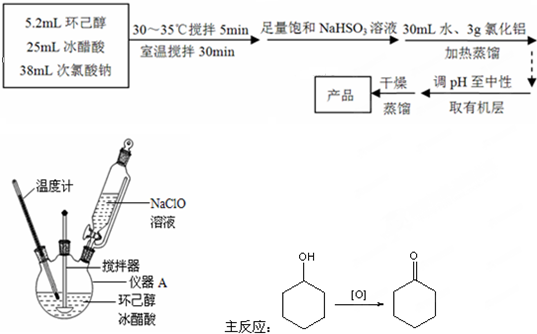
(1)步骤①可在如图装置中进行,仪器A的名称是三颈烧瓶;
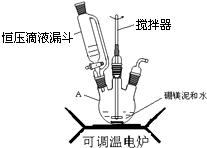
(2)本实验中多次用到抽滤,相比普通过滤,抽滤的优点是速度快、得到的滤渣较干燥;
(3)步骤②中加硼镁泥的作用是消耗多余的硫酸使pH增加到5~6,促使Fe3+、Al3+完全沉淀,NaClO的作用是氧化Fe2+、Mn2+;
(4)步骤③趁热过滤的目的是防止析出MgSO4•7H2O该过程中温度应控制在80℃左右;
(5)步骤④的具体操作:当出现晶膜时即停止加热,其原因是防止MgSO4•7H2O失去结晶水.
| A. | 0-10min内,用A表示的平均反应速率是0.05mol•L-1•min-1 | |
| B. | 0-10min内,用B表示的平均反应速率是0.01mol•L-1•min-1 | |
| C. | 分别用B、C、D表示反应的速率,其比值是4:3:1 | |
| D. | 随着反应的进行,容器内气体压强始终保持不变 |
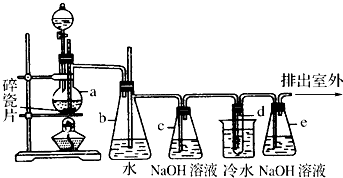

 某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线: