题目内容
16.下列物质中既能与盐酸反应,又能与氢氧化钠溶液反应的组合是( )①(NH4)2CO3 ②Al2O3 ③Cu(OH)2 ④Al(OH)3 ⑤Na2CO3 ⑥NaHCO3.
| A. | ①②⑤ | B. | ②④⑥ | C. | ①②④⑥ | D. | ①②④⑤ |
分析 根据物质间的反应进行判断,中学常见的既能与酸反应又能与碱反应的物质主要有:
①两性物质:Al2O3、ZnO、Al(OH)3、Zn(OH)2、氨基酸、蛋白质等;
②多元弱酸的酸式盐:NaHCO3、KHS、KHSO3、NaH2PO4等;
③弱酸的铵盐及其酸式盐:(NH4)2S、NH4HS、(NH4)2CO3、NH4HCO3、CH3COONH4等;
④某些具有两性的金属:Zn、Al等;
⑤某些非金属:Si、S等;
⑥其它一些物质.如:a、某些盐类物质既与酸反应,又与碱反应;
b、个别酸性氧化物SiO2;
c、具有还原性的无氧酸:H2S、HI等与氧化性酸反应、与碱反应;
d、具有氧化性酸:浓H2SO4、HNO3等与还原性酸反应、与碱反应.以此解答本题.
解答 解:①(NH4)2CO3 既能与盐酸反应生成二氧化碳,又能和碱反应生成氨气,故①正确;
②Al2O3属于两性氧化物,既能与酸反应,生成铝盐(Al3+),又能与碱反应生成偏铝酸盐(AlO2-),故②正确;
③Cu(OH)2 与盐酸反应,不氢氧化钠反应,故③错误;
④Al(OH)3 属于两性氢氧化物,既能与酸反应,生成铝盐(Al3+),又能与碱反应生偏铝酸盐(AlO2-),故④正确;
⑤Na2CO3与盐酸反应生成二氧化碳,不与氢氧化钠反应,故⑤错误;
⑥NaHCO3属于弱酸弱碱盐,既能与盐酸反应,生成CO2气体,又能与氢氧化钠反应,生成盐,故⑥正确;
故选C.
点评 本题考查元素化合物的性质,题目难度不大,旨在考查学生对知识的理解识记与知识归纳,注意基础知识的积累.

练习册系列答案
相关题目
6.下列各操作中,正确的是( )
| A. | 为减缓反应速率,用饱和食盐水与电石反应制乙炔 | |
| B. | 进行酸碱中和滴定时,锥形瓶应用待测液润洗 | |
| C. | 实验室制乙烯时应将无水乙醇缓慢加入浓硫酸中,并加入碎瓷片以防爆沸 | |
| D. | 配制FeCl3溶液时,加入少量稀硫酸抑制其水解 |
7.在稀硫酸与锌的反应中,硫酸是( )
| A. | 是氧化剂 | B. | 是还原剂 | C. | 被氧化 | D. | 催化剂 |
4.下列叙述错误的是( )
| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用高锰酸钾酸性溶液可区分己烷和3-己烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用溴水或酸性高锰酸钾溶液可以鉴别1-己烯和乙醛 |
11.下列变化中,属于物理变化的是( )
| A. | 煤干馏 | B. | 石油的减压分馏 | C. | 石油裂解 | D. | 煤液化 |
1.金融危机之下,中国铝工业受到了巨大的冲击.2009年6月30日至7月2日在上海新国际博览中心举办的中国国际铝工业展览会却提出了“展现铝业盎然生机”的口号,成为全球铝业的焦点和亮点.某化学兴趣小组的同学们决定铝及其化合物的性质比较展开探究活动.搜索到的一些实验数据如下:
铝及其氧化物的有关实验数据如下:
(1)将铝片插入硝酸汞溶液中,铝片表面灰暗,用湿布擦试后,铝片上附着了液态银白色的物质.将该铝片静置一段时间,铝片表面长出白色须状物,手持铝片时,白色须状物脱落,铝片发烫.经实验白色须状物能溶于稀盐酸且无气体放出.试写出直接导致铝片发烫的热化学反应方程式4Al(s)+3O2(g)=2Al2O3(s),△H=-2408KJ/mol.
(2)剪长约6cm、宽2cm的铜片、铝片各一片,分别用接线柱平行地固定在一块塑料板上(间隔2cm).将铜片与铝片分别和电流表的“+”、“-”端相连接,电流表指针调到中间位置.取两个50mL的小烧杯,在一个烧杯中注入约40mL的浓硝酸,在另一只烧杯中注入40mL0.5mol/L的硫酸溶液.试回答下列问题:
①两电极同时插入稀硫酸中,电流表指针偏向铝(填“铝”或“铜”)极,铝片上电极反应式为Al-3e-=Al3+;
②两电极同时插入浓硝酸时,电流表指针偏向铜(填“铝”或“铜”)极,此时铝是正(填“正”或“负”)极,铝片上电极反应式为2NO3-+2e-+4H+=2NO2↑+2H2O.
(3)能源问题是人们关心的热点,有人提出用金属铝作燃料,这真是一种大胆而新颖的设想.对此,你的观点是B(填“A”或“B”),其理由是工业上用电解氧化铝的方法制取铝,要消耗大量的电能.A.可行B.不可行.
铝及其氧化物的有关实验数据如下:
| 熔点/℃ | 沸点/℃ | 燃烧热/kJ•mol-1 | |
| 铝 | 660 | 2467 | 602 |
| 氧化铝 | 2050 | 2980 | / |
(2)剪长约6cm、宽2cm的铜片、铝片各一片,分别用接线柱平行地固定在一块塑料板上(间隔2cm).将铜片与铝片分别和电流表的“+”、“-”端相连接,电流表指针调到中间位置.取两个50mL的小烧杯,在一个烧杯中注入约40mL的浓硝酸,在另一只烧杯中注入40mL0.5mol/L的硫酸溶液.试回答下列问题:
①两电极同时插入稀硫酸中,电流表指针偏向铝(填“铝”或“铜”)极,铝片上电极反应式为Al-3e-=Al3+;
②两电极同时插入浓硝酸时,电流表指针偏向铜(填“铝”或“铜”)极,此时铝是正(填“正”或“负”)极,铝片上电极反应式为2NO3-+2e-+4H+=2NO2↑+2H2O.
(3)能源问题是人们关心的热点,有人提出用金属铝作燃料,这真是一种大胆而新颖的设想.对此,你的观点是B(填“A”或“B”),其理由是工业上用电解氧化铝的方法制取铝,要消耗大量的电能.A.可行B.不可行.
8.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,2.0 g氟化氢所含电子数为0.1NA | |
| B. | 1 mol Na2O2 跟足量H2O反应时得到电子的数目为2NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |
5.某烃C15H24分子结构非常对称,实验证明该烃仅存在三种基团:乙烯基(CH2=CH-)、亚甲基(-CH2-)、次甲基(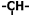 ),并且乙烯基和次甲基之间必须通过亚甲基相连,当该烃含有单环结构是分子中的乙烯基和亚甲基的个数依次为( )
),并且乙烯基和次甲基之间必须通过亚甲基相连,当该烃含有单环结构是分子中的乙烯基和亚甲基的个数依次为( )
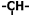 ),并且乙烯基和次甲基之间必须通过亚甲基相连,当该烃含有单环结构是分子中的乙烯基和亚甲基的个数依次为( )
),并且乙烯基和次甲基之间必须通过亚甲基相连,当该烃含有单环结构是分子中的乙烯基和亚甲基的个数依次为( )| A. | 2个,3个 | B. | 5个,3个 | C. | 4个,6个 | D. | 3个,6个 |
6.化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显.影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:
因素一:银氨溶液的pH大小;
因素二:反应(水浴)的温度.
②你设计实验验证上述“因素一”,完成下表中内容.
提供试剂:乙醛、2%稀氨水、0.25mol/L NaOH溶液、盐酸、2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
③请写出乙醛发生银镜反应的化学方程式:CH3CHO+2Ag(NH3)2OH$\stackrel{水浴加热}{→}$CH3COONH4+2Ag↓+3NH3+H2O.
①猜想:
因素一:银氨溶液的pH大小;
因素二:反应(水浴)的温度.
②你设计实验验证上述“因素一”,完成下表中内容.
提供试剂:乙醛、2%稀氨水、0.25mol/L NaOH溶液、盐酸、2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
| 实验 步骤 | 实验操作 | 预期现象及结论 (步骤1只写现象) |
| 1 | 在A、B两支洁净的试管中各加入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水, 至沉淀恰好溶解,此时制得pH均约为8的银氨溶液. | 先生成白色沉淀,后沉淀溶解. |
| 2 | 往A、B试管加入3滴乙醛,然后在A试管中加1滴NaOH溶液;振荡后将两支试管放在热水浴中温热. | 若A试管比B试管出现的银镜时间短、光亮,则则溶液pH大,反应速率快; 若A试管比B试管出现的银镜时间长,则则溶液pH大,反应速率慢. |