题目内容
4.下列叙述错误的是( )| A. | 用金属钠可区分乙醇和乙醚 | |
| B. | 用高锰酸钾酸性溶液可区分己烷和3-己烯 | |
| C. | 用水可区分苯和溴苯 | |
| D. | 用溴水或酸性高锰酸钾溶液可以鉴别1-己烯和乙醛 |
分析 A.钠和乙醇反应生成氢气,和乙醚不反应;
B.己烷和酸性高锰酸钾溶液不反应,3-己烯能被酸性高锰酸钾溶液氧化;
C.水和苯、溴苯都不互溶,但苯密度小于水,溴苯密度大于水;
D.1-己烯和乙醛都能与溴水、酸性高锰酸钾溶液反应.
解答 解:A.钠和乙醇反应生成氢气,和乙醚不反应,现象不同,可以鉴别,故A正确;
B.己烷和酸性高锰酸钾溶液不反应,3-己烯能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,所以现象不同,可以鉴别,故B正确;
C.水和苯、溴苯都不互溶,但苯密度小于水,溴苯密度大于水,所以混合时现象不同,可以鉴别,故C正确;
D.1-己烯和乙醛都能与溴水、酸性高锰酸钾溶液反应,所以都能使溴水、酸性高锰酸钾溶液褪色,现象相同,不能鉴别,故D错误;
故选D.
点评 本题考查有机物鉴别,侧重考查学生分析判断能力,明确官能团及其性质关系是解本题关键,易错选项是D,注意醛基能被溴、酸性高锰酸钾溶液氧化.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
12.下列各离子组中,在溶液中能够大量共存的一组是( )
| A. | AlO2-、SO42-、Cl-、K+ | B. | Al3+、Ca2+、HCO3-、Na+ | ||
| C. | Fe3+、NH4+、SO42-、SCN- | D. | H+、Cl-、Na+、HS- |
19.X、Y、Z、R分别代表四种元素,如果aXm+、bYn+、cZn-、dRm- 四种离子的电子层结构相同,则下列关系式正确的是( )
| A. | a-c=m-n | B. | a-b=n-m | C. | c+d=m+n | D. | b-d=n+m |
9.判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示
(1)亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推出它们的结构式分别为 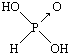 和
和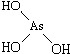 ,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:①H3PO3+2NaOH=Na2HPO3+2H2O; ②H3AsO3+3NaOH=Na3AsO3+3H2O.
| 名称 | 次氯酸 | 磷酸 | 硫酸 | 高氯酸 |
| 结构式 | Cl-OH |  | 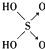 | 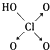 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 和
和 ,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:①H3PO3+2NaOH=Na2HPO3+2H2O; ②H3AsO3+3NaOH=Na3AsO3+3H2O.
16.下列物质中既能与盐酸反应,又能与氢氧化钠溶液反应的组合是( )
①(NH4)2CO3 ②Al2O3 ③Cu(OH)2 ④Al(OH)3 ⑤Na2CO3 ⑥NaHCO3.
①(NH4)2CO3 ②Al2O3 ③Cu(OH)2 ④Al(OH)3 ⑤Na2CO3 ⑥NaHCO3.
| A. | ①②⑤ | B. | ②④⑥ | C. | ①②④⑥ | D. | ①②④⑤ |
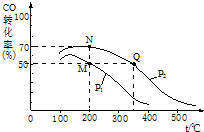 减少污染、保护环境是全世界最热门的课题.
减少污染、保护环境是全世界最热门的课题. CaCl2
CaCl2 N2
N2 OH-
OH-
 .
.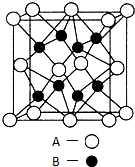 A、B、C、D、E是元素周期表中原子序数依次递增的前四周期元素.A原子最外层电子数为内层电子数的3倍;B的焰色反应呈黄色;C的氢化物是一种强酸,其浓溶液可与A、E的化合物反应生成C的单质;D是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题:
A、B、C、D、E是元素周期表中原子序数依次递增的前四周期元素.A原子最外层电子数为内层电子数的3倍;B的焰色反应呈黄色;C的氢化物是一种强酸,其浓溶液可与A、E的化合物反应生成C的单质;D是一种金属元素,其基态原子中有6个未成对电子.请回答下列问题: