题目内容
1.金融危机之下,中国铝工业受到了巨大的冲击.2009年6月30日至7月2日在上海新国际博览中心举办的中国国际铝工业展览会却提出了“展现铝业盎然生机”的口号,成为全球铝业的焦点和亮点.某化学兴趣小组的同学们决定铝及其化合物的性质比较展开探究活动.搜索到的一些实验数据如下:铝及其氧化物的有关实验数据如下:
| 熔点/℃ | 沸点/℃ | 燃烧热/kJ•mol-1 | |
| 铝 | 660 | 2467 | 602 |
| 氧化铝 | 2050 | 2980 | / |
(2)剪长约6cm、宽2cm的铜片、铝片各一片,分别用接线柱平行地固定在一块塑料板上(间隔2cm).将铜片与铝片分别和电流表的“+”、“-”端相连接,电流表指针调到中间位置.取两个50mL的小烧杯,在一个烧杯中注入约40mL的浓硝酸,在另一只烧杯中注入40mL0.5mol/L的硫酸溶液.试回答下列问题:
①两电极同时插入稀硫酸中,电流表指针偏向铝(填“铝”或“铜”)极,铝片上电极反应式为Al-3e-=Al3+;
②两电极同时插入浓硝酸时,电流表指针偏向铜(填“铝”或“铜”)极,此时铝是正(填“正”或“负”)极,铝片上电极反应式为2NO3-+2e-+4H+=2NO2↑+2H2O.
(3)能源问题是人们关心的热点,有人提出用金属铝作燃料,这真是一种大胆而新颖的设想.对此,你的观点是B(填“A”或“B”),其理由是工业上用电解氧化铝的方法制取铝,要消耗大量的电能.A.可行B.不可行.
分析 (1)根据铝燃烧发热书写热化学反应方程式;
(2)①该原电池中,铝易失电子作负极,铜作正极,电子从铝沿导线流向铜,电流计指针偏向失电子的电极;
②在浓硝酸中,铝被钝化,铜溶解,所以铜易失电子为负极,铝是正极,电流计指针偏向失电子的电极;
(3)工业上用电解氧化铝的方法制取铝,要消耗大量的电能,不能缓解能源紧张.
解答 解:(1)铝燃烧发热,并且铝的燃烧热为602kJ•mol-1,所以导致铝片发烫的热化学反应方程式为:4Al(s)+3O2(g)=2Al2O3(s),△H=-2408KJ/mol,故答案为:4Al(s)+3O2(g)=2Al2O3(s),△H=-2408KJ/mol;
(2)①该原电池中,铝易失电子作负极,铜作正极,负极上铝失电子发生氧化反应,电极反应式为:Al-3e-=Al3+,电流计指针偏向失电子的电极,所以电流计指针偏向铝,
故答案为:铝;Al-3e-=Al3+;
②该原电池中,铝和浓硝酸发生钝化现象而阻止进一步反应,铜易和浓硝酸反应,所以铜易失电子而作负极,铝作正极,电流计指针偏向失电子的电极铜,铜电极上失电子发生氧化反应,电极反应式为:Cu-2e-=Cu2+,正极上硝酸根离子得电子生成二氧化氮,电极反应式为:2NO3-+2e-+4H+=2NO2↑+2H2O,
故答案为:铜;正,2NO3-+2e-+4H+=2NO2↑+2H2O;
(3)工业上用电解氧化铝的方法制取铝,要消耗大量的电能,不能缓解能源紧张;铝作为民用新型能源,不可行.
故答案为:B;工业上用电解氧化铝的方法制取铝,要消耗大量的电能.
点评 考查铝及化合物性质,比较基础,注意基础知识掌握,(3)中对方案、设想进行评价,是一道开放性问题、社会性问题,是对学生综合能力考查.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
12.下列各离子组中,在溶液中能够大量共存的一组是( )
| A. | AlO2-、SO42-、Cl-、K+ | B. | Al3+、Ca2+、HCO3-、Na+ | ||
| C. | Fe3+、NH4+、SO42-、SCN- | D. | H+、Cl-、Na+、HS- |
9.判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示
(1)亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推出它们的结构式分别为 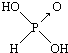 和
和 ,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:①H3PO3+2NaOH=Na2HPO3+2H2O; ②H3AsO3+3NaOH=Na3AsO3+3H2O.
| 名称 | 次氯酸 | 磷酸 | 硫酸 | 高氯酸 |
| 结构式 | Cl-OH | 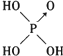 | 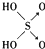 |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 和
和 ,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性
,二者酸性强弱原因亚磷酸含有1个非羟基氧原子,而亚砷酸没有非羟基氧原子,故亚磷酸的酸性强于亚砷酸的酸性(2)亚磷酸和亚砷酸与过量的氢氧化钠溶液反应的化学方程式分别为:①H3PO3+2NaOH=Na2HPO3+2H2O; ②H3AsO3+3NaOH=Na3AsO3+3H2O.
16.下列物质中既能与盐酸反应,又能与氢氧化钠溶液反应的组合是( )
①(NH4)2CO3 ②Al2O3 ③Cu(OH)2 ④Al(OH)3 ⑤Na2CO3 ⑥NaHCO3.
①(NH4)2CO3 ②Al2O3 ③Cu(OH)2 ④Al(OH)3 ⑤Na2CO3 ⑥NaHCO3.
| A. | ①②⑤ | B. | ②④⑥ | C. | ①②④⑥ | D. | ①②④⑤ |
6.2008年北京奥运会的“祥云”火炬所用燃料的主要成分是丙烷,下列有关丙烷的叙述正确的是( )
| A. | 丙烷的分子式是C3H6 | |
| B. | 丙烷分子中的碳原子在一条直线上 | |
| C. | 丙烷在光照条件下能够发生取代反应 | |
| D. | 丙烷的熔点比乙烷低 |
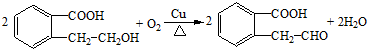 .
.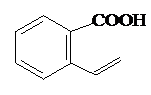 或
或 .
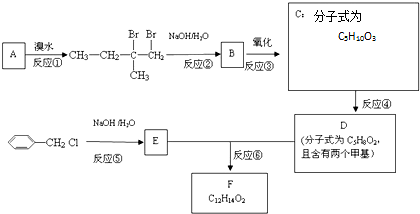
.
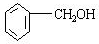 ;
;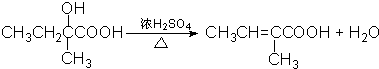 ;
;
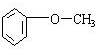 .
.