题目内容
8.NA为阿伏加德罗常数,下列说法正确的是( )| A. | 常温常压下,2.0 g氟化氢所含电子数为0.1NA | |
| B. | 1 mol Na2O2 跟足量H2O反应时得到电子的数目为2NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子数为3NA |
分析 A、求出HF的物质的量,然后根据HF为10电子分子来计算;
B、过氧化钠与水的反应为歧化反应;
C、标况下,二氯甲烷为液态;
D、乙烯、丙烯和丁烯的最简式均为CH2.
解答 解:A、2.0gHF的物质的量n=$\frac{2.0g}{20g/mol}$=0.1mol,而HF为10电子分子,故0.1molHF中含1mol电子,即NA个,故A错误;
B、过氧化钠与水的反应为歧化反应,1mol过氧化钠与水反应时只得1mol电子,即NA个,故B错误;
C、标况下,二氯甲烷为液态,故不能根据气体摩尔体积来计算,故C错误;
D、乙烯、丙烯和丁烯的最简式均为CH2,故14g混合物中含有的CH2的物质的量n=$\frac{14g}{14g/mol}$=1mol,则含有3mol原子,即3NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,根据物质的结构、状态和公式来计算,难度不大.

练习册系列答案
相关题目
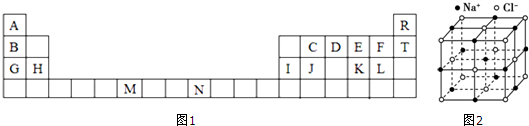
18.下表为元素周期表的一部分,表中列出10种元素在周期表中的位置,按要求回答下列各题
(1)化学性质最不活泼的元素符号是Ne,金属性最强的单质与水反应的化学方程式是2K+2H2O=2KOH+H2↑.
(2)画出④形成的简单离子的结构示意图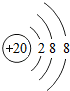 .
.
(3)①③⑤三种元素最高价氧化物的水化物中碱性最强的物质的化学式是NaOH.
(4)元素①形成的稳定的氧化物在呼吸面具中供氧时的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑.
(5)③⑤⑦三种元素形成的简单离子,离子半径由大到小的顺序是O2->Mg2+>Al3+.
(6)设计一个简单实验证明⑧⑨两种元素非金属性强弱的比较将氯气通入Na2S溶液中,如果溶液中出现浅黄色沉淀,就说明氯气的氧化性大于硫,则非金属性Cl>S.
 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | ⑦ | ⑩ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑨ | |||
| 4 | ② | ④ |
(2)画出④形成的简单离子的结构示意图
 .
.(3)①③⑤三种元素最高价氧化物的水化物中碱性最强的物质的化学式是NaOH.
(4)元素①形成的稳定的氧化物在呼吸面具中供氧时的化学方程式是:2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑.
(5)③⑤⑦三种元素形成的简单离子,离子半径由大到小的顺序是O2->Mg2+>Al3+.
(6)设计一个简单实验证明⑧⑨两种元素非金属性强弱的比较将氯气通入Na2S溶液中,如果溶液中出现浅黄色沉淀,就说明氯气的氧化性大于硫,则非金属性Cl>S.
19.X、Y、Z、R分别代表四种元素,如果aXm+、bYn+、cZn-、dRm- 四种离子的电子层结构相同,则下列关系式正确的是( )
| A. | a-c=m-n | B. | a-b=n-m | C. | c+d=m+n | D. | b-d=n+m |
16.下列物质中既能与盐酸反应,又能与氢氧化钠溶液反应的组合是( )
①(NH4)2CO3 ②Al2O3 ③Cu(OH)2 ④Al(OH)3 ⑤Na2CO3 ⑥NaHCO3.
①(NH4)2CO3 ②Al2O3 ③Cu(OH)2 ④Al(OH)3 ⑤Na2CO3 ⑥NaHCO3.
| A. | ①②⑤ | B. | ②④⑥ | C. | ①②④⑥ | D. | ①②④⑤ |
18.CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( )
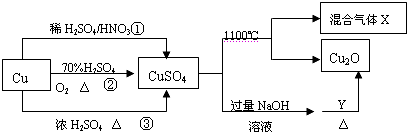

| A. | 1mol CuSO4在1100℃所得混合气体X中O2可能为0.75mol(X的组成为SO2、SO3、O2) | |
| B. | 相对于途径①、②,途径③更好地体现了绿色化学理念 | |
| C. | 途径①所用混酸中H2SO4与HNO3物质的量之比最好为3:2 | |
| D. | Y一定是葡萄糖 |
 .
.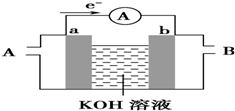 (1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH. 请回答下列问题:
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O $?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH. 请回答下列问题: