题目内容
5.NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 1mol Fe粉与1mol水蒸气充分反应转移的电子数为3NA | |
| B. | 电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜 | |
| C. | 6.8克熔融的KHSO4混中含有0.1NA个阳离子 | |
| D. | 标准状况下,11.2L四氯化碳所含分子数为0.5NA |
分析 A、1mol Fe粉与1mol水蒸气充分反应生成四氧化三铁和氢气,3Fe+4H2O=Fe3O4+4H2铁过量水蒸不够,所以1mol水蒸气完全反应;
B、电解精炼铜时,阴极是铜离子放电,若转移了NA个电子,有0.5mol铜单质生成;
C、熔融硫酸氢钾电离出钾离子和硫酸氢根离子;
D、标况下,四氯化碳为液态.
解答 解:A、1mol Fe粉与1mol水蒸气充分反应生成四氧化三铁和氢气,3Fe+4H2O=Fe3O4+4H2铁过量水蒸不够,所以1mol水蒸气完全反应,1mol水蒸气充分反应转移的电子数为2NA,故A错误;
B、电解精炼铜时,阴极是铜离子放电,若转移了NA个电子,有0.5mol铜单质生成,质量为0.5mol×64g/mol=32g,故B正确;
C、6.8g熔融的KHSO4的物质的量0.05mol,0.05mol熔融硫酸氢钾能够电离出0.05mol钾离子和0.05mol硫酸氢根离子,所以含有的阳离子数为0.05NA,故C错误;
D、标况下,四氯化碳为液态,不能根据气体摩尔体积来计算其物质的量,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案
相关题目
13.二氧化碳气体中含有少量氯化氢杂质,若要除杂,最好选用( )
| A. | 饱和碳酸钠溶液 | B. | 浓硫酸 | ||
| C. | 饱和碳酸氢钠溶液 | D. | 饱和石灰水 |
10.下列有关溶液中粒子浓度关系的比较中不正确的是( )
| A. | 醋酸溶液中离子浓度的关系满足:c(H+)═c(OH-)+c(CH3COO-) | |
| B. | 用0.100 0 mol•L-1NaOH滴定未知浓度的CH3COOH溶液,恰好反应时:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| C. | pH=2的HA溶液与pH=12的MOH溶液以任意比混合:c(H+)+c(M+)═c(OH-)+c(A-) | |
| D. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)═c(Na+) |
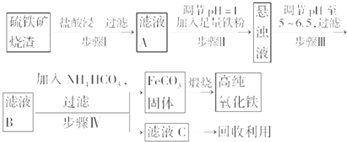

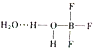 硼元素在化学中很重要的地位,硼及其化合物广泛应用于水磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用.
硼元素在化学中很重要的地位,硼及其化合物广泛应用于水磁材料、超导材料、富燃料材料、复合材料等高新材料领域应用.