题目内容
16.由Cu、N、B、Ni等元素组成的新型材料有着广泛用途.
(1)基态 Cu+的最外层电子排布式为3s23p63d10.
(2)研究者预想合成一个纯粹由氮组成的新物种 N5+ 与N3-,若N5+ 离子中每个氮原子均满足8电子且呈对称结构,以下有关推测正确的是CD
A.N5+有24个电子
B. N5+离子中存在三对未成键的电子对
C. N5+阳离子中存在两个氮氮三键
D.N3-离子的空间构型为直线形
(3)化合物A(H3BNH3)是一种潜在储氢材料,它可由六元环状化合物(HB=NH)3通过3CH4+2(HB=NH)3+6H2O═3CO2+6H3BNH3 制得.
①与上述化学方程式有关的叙述不正确的是A.(填标号)
A.反应前后碳原子的轨道杂化类型不变
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形
C.第一电离能:N>O>C>B
D.化合物A中存在配位键
②1个(HB=NH)3 分子中有12个σ 键.
③Na与Cl形成的晶体很脆,经不起锤击,Si与O形成的晶体同样很脆,也经不起锤击,然而二者的摩氏硬度却相差极大,请解释摩氏硬度相差大的原因氯化钠属于离子晶体,阴阳离子通过离子键相互作用,二氧化硅属于原子晶体,原子之间以共价键相互结合形成空间立体网状结构.
(4)在硼酸盐中,阴离子有链状、环状等多种结构形式.图1(a)是一种链状结构的多硼酸根,则多硼酸根离子符号为[BO2]nn-(或BO2-)图1(b)是硼砂晶体中阴离子的环状结构,其中硼原子采取的杂化类型为sp2、sp3.
(5)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为acm,则该晶体中距离最近的两个阳离子核间的距离为$\frac{\sqrt{2}}{2}$acm(用含有a的代数式表示).在一定温度下,NiO晶体可以自发地分散并形成“单分子层”(如图2),可以认为氧离子作密置单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为1.83×10-3g(氧离子的半径为1.40×10-10m,$\sqrt{3}$≈l.732).
分析 (1)Cu+基态核外电子排布式1s22s22p63s23p63d10;
(2)A.阳离子核外电子数=质子总数-电荷数;
B.N5+ 离子中每个氮原子均满足8电子且呈对称结构,N5+离子的结构为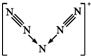 ,中间N原子有2对孤对电子;
,中间N原子有2对孤对电子;
C.根据B中分析判断;
D.N3-离子与二氧化碳分子核外等电子体;
(3)①A.由方程式可知:碳元素由CH4变为CO2,碳原子杂化类型由sp3转化为sp;
B.CH4、H2O、CO2分子空间构型分别是:正四面体形、V形、直线形;
C.同周期随原子序数增大,第一电离能呈增大趋势,ⅡA族、ⅤA族元素第一电离能共有同周期相邻元素;
D.一般是形成3个键,(H3BNH3)由六元环状化合物(HB=NH)3通过3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得,其中1个键是配位键;
②1个(HB=NH)3分子中硼原子与氮原子间以σ键结合,而剩余的p轨道形成一个共轭大π键,B-H键有3个,N-H键有3个,B-N有σ键有6个;
③氯化钠属于离子晶体,二氧化硅属于原子晶体;
(4)1个B原子连接3个O原子,其中2个氧原子分别为2个B原子共有,利用均摊法计算每个B原子连接O原子数目,进而确定多硼酸根离子符号;
硼砂晶体中存在形成2个σ键、3个σ键的B原子,B原子最外层电子数全部处于成键;
(5)根据氯化钠的结构知,氧离子和相邻的镍离子之间的距离为$\frac{1}{2}$a,距离最近的两个阳离子核间的距离是距离最近的氧离子和镍离子距离的$\sqrt{2}$倍;
根据图片知,每个氧化镍所占的面积=(2×1.40×10-10m)×(2×1.40×10-10m×sin60°),每个氧化镍的质量=$\frac{74.7}{{N}_{A}}$g,每个氧化镍的质量乘以每平方米含有的氧化镍个数就是每平方米含有的氧化镍质量.
解答 解:(1)Cu+基态核外电子排布式1s22s22p63s23p63d10,基态 Cu+的最外层电子排布式为:3s23p63d10,
故答案为:3s23p63d10;
(2)A.1个氮原子中含有7个电子,则1个N5分子中含有35个电子,N5+是由N5分子失去1个电子得到的,则1个N5+粒子中有34个电子,故A错误;
B.N5+ 离子中每个氮原子均满足8电子且呈对称结构,N5+离子的结构为 ,中间N原子有2对孤对电子,有4对未成键的电子对,故B错误;
,中间N原子有2对孤对电子,有4对未成键的电子对,故B错误;
C.N5+离子的结构为 ,则N5+阳离子中存在两个氮氮三键,故C正确;
,则N5+阳离子中存在两个氮氮三键,故C正确;
D.N3-离子与二氧化碳分子核外等电子体,为直线型结构,故D正确;
故选:CD;
(3)①A.由方程式可知:碳元素由CH4变为CO2,碳原子杂化类型由sp3转化为sp,故A错误;
B.CH4分子中价层电子对=σ 键电子对+中心原子上的孤电子对=4+$\frac{1}{2}$×(4-4×1)=4,且不含孤电子对,所以其空间构型是正四面体,H2O中价层电子对个数=2+$\frac{1}{2}$×(6-2×1)=4,且含有2个孤电子对,所以H2O的VSEPR模型为四面体,分子空间构型为V型,、CO2分子中价层电子对=σ 键电子对+中心原子上的孤电子对=2+$\frac{1}{2}$×(4-2×2)=2,所以二氧化碳是直线型结构,故B正确;
C.同周期随原子序数增大,第一电离能呈增大趋势,ⅡA族、ⅤA族元素第一电离能共有同周期相邻元素,故所以它们的第一电离能大小顺序是I1(N)>I1(O)>I1(C)>I1(B),故C正确;
D.一般是形成3个键,(H3BNH3)由六元环状化合物(HB=NH)3通过3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得,其中1个键是配位键,故D正确,
故选:A;
②1个(HB=NH)3分子中硼原子与氮原子间以σ键结合,而剩余的p轨道形成一个共轭大π键,B-H键有3个,N-H键有3个,B-N有σ键有6个,故一共12个,
故答案为:12;
③氯化钠属于离子晶体,阴阳离子通过离子键相互作用,二氧化硅属于原子晶体,原子之间以共价键相互结合形成空间立体网状结构,故二者莫氏硬度相差较大,
故答案为:氯化钠属于离子晶体,阴阳离子通过离子键相互作用,二氧化硅属于原子晶体,原子之间以共价键相互结合形成空间立体网状结构;
(4)1个B原子连接3个O原子,其中2个氧原子分别为2个B原子共有,则每个B原子实际结合O原子数目为1+2×$\frac{1}{2}$=2,代一个单位负电荷,故多硼酸根化学式为:[BO2]nn-(或BO2-),
硼砂晶体中存在形成2个σ键、3个σ键的B原子,B原子最外层电子数全部处于成键,故B原子采取sp2、sp3杂化,
故答案为:[BO2]nn-(或BO2-);sp2、sp3;
(5)根据氯化钠的结构知,氧离子和相邻的镍离子之间的距离为$\frac{1}{2}$a,距离最近的两个阳离子核间的距离是距离最近的氧离子和镍离子距离的$\sqrt{2}$倍,所以其距离是 $\frac{\sqrt{2}}{2}$acm;
根据图片知,每个氧化镍所占的面积=(2×1.40×10-10m)×(2×1.40×10-10m×sin60°)=4×1.40×10-10×1.40×10-10×sin60°m2,则每平方米含有的氧化镍个数=$\frac{1}{4×1.4×1{0}^{-10}×1.4×1{0}^{-10}×sin60°}$,每个氧化镍的质量=$\frac{74.7}{{N}_{A}}$g,所以每平方米含有的氧化镍质量=$\frac{74.7}{{N}_{A}}$g×$\frac{1}{4×1.4×1{0}^{-10}×1.4×1{0}^{-10}×sin60°}$,=1.83×10-3,
故答案为:$\frac{\sqrt{2}}{2}$a;1.83×10-3.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、电离能、空间结构、化学键、杂化轨道、晶体结构与计算等,(5)中注意计算“1NiO”的体积应包含孔隙体积,难度较大.

 名校课堂系列答案
名校课堂系列答案| A. | NH3→NH4+ | B. | N2→NH3 | C. | NH3→NO | D. | Cl2→Cl- |
①将某卤代烃与氢氧化钠的水溶液共热,向冷却后的反应液中滴加AgNO3溶液,若产生白色沉淀,则证明该卤代烃为氯代烃
②用乙醇和30%的硫酸共热到170℃制取乙烯
③在苯酚中滴入少量溴水出现白色沉淀
④将苯与浓硝酸混合加热至60℃制备硝基苯
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,再加入银氨溶液加热.
| A. | ①③④ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①②③④⑤ |
| A. | Cl2>Fe3+>I2>S | B. | S>I2>Fe3+>Cl2 | C. | Fe3+>Cl2>H2S>I2 | D. | Cl2>I2>Fe3+>H2S |
| A. | Al2(SO4)3 | B. | FeCl3 | C. | Na2CO3 | D. | KCl |
| A. | 碘与干冰分别受热变为气体 | B. | 硝酸铵与硝酸分别受热变为气体 | ||
| C. | 氯化钠与氯化氢分别溶解在水中 | D. | 氧化铝与冰分别受热熔化 |
| A. | 1mol Fe粉与1mol水蒸气充分反应转移的电子数为3NA | |
| B. | 电解精炼铜时,若转移了NA个电子,则阴极析出32 g铜 | |
| C. | 6.8克熔融的KHSO4混中含有0.1NA个阳离子 | |
| D. | 标准状况下,11.2L四氯化碳所含分子数为0.5NA |