题目内容
【题目】工业上乙醚可用于制造无烟火药。实验室合成乙醚的原理如下:2CH3CH2OH![]() CH3CH2OCH2CH3+H2O。
CH3CH2OCH2CH3+H2O。
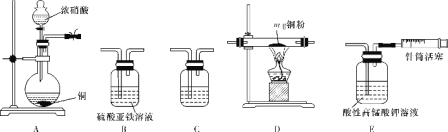
(乙醚制备)装置设计如图(部分装置略)
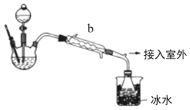
(1)仪器b应更换为下列的___(填序号)。
A.干燥器 B.直形冷凝管 C.玻璃管 D.安全瓶
(2)反应温度控制在145℃,还需添加___以防止局部过热,若温度过高,会生成一种能催熟果实的气体,则副反应化学方程式为:___。
(3)反应时,若滴入乙醇的速率显著超过馏出液速率,反应速率会降低,可能原因是___。
(乙醚提纯)
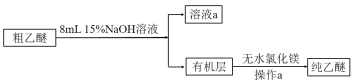
(4)粗乙醚中含有的主要杂质为___;操作a的名称是___;无水氯化镁的作用是___。
【答案】B 沸石或碎瓷片 CH3CH2OH![]() CH2=CH2↑+H2O 温度骤降导致反应速率降低 乙醇 蒸馏 干燥乙醚
CH2=CH2↑+H2O 温度骤降导致反应速率降低 乙醇 蒸馏 干燥乙醚
【解析】
(1)仪器b是球形冷凝管,可以更换为直行冷凝管;
(2)防止局部过热,一般选择沸石或者碎瓷片,温度过高时会生成的催熟果实的气体是乙烯,那么副反应为:CH3CH2OH![]() CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
(3)乙醇的速率明显的超过流出液体的速率的时候,降低温度反应速率会降低;
(4)将粗乙醚当中加入氢氧化钠溶液洗涤逸出的乙醇,可以得到含氢氧化钠的乙醇溶液,然后加入无水氯化镁来吸收水蒸气,有机层采用蒸馏的方法进行分离提纯。

练习册系列答案
相关题目