题目内容
7.已知四种元素的原子半径如表所示:| 元素 | N | S | O | Si |
| 原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
| A. | 0.80×10-10m | B. | 1.20×10-10m | C. | 1.10×10-10m | D. | 0.70×10-10m |
分析 同周期自左而右原子半径减小,同主族自上而下原子半径增大.
解答 解:N、P是同一主族元素,P元素的原子序数大于N元素的原子序数,所以原子半径:r(P)>0.75×10-10m;
Si、P、S是同一周期的元素,且P的原子序数大于Si的原子序数小于S的原子序数,所以原子半径:1.02×10-10m<r(P)<1.17×10-10m,
故磷元素的原子半径可能为1.10×10-10m,
故选C.
点评 本题考查了微粒半径大小的比较,难度不大,注意对元素周期律的理解,注意电子层结构相同的离子半径大小的比较方法.

练习册系列答案
相关题目
3.25℃时,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:Na+、NH4+、SO42-、ClO- | |
| B. | KW/c(H+)=0.1 mol•L-1的溶液中:Na+、K+、MnO4-、HCO3- | |
| C. | 0.1 mol•L-1的Na2SO3溶液中:K+、H+、SO42-、NO3- | |
| D. | 澄清透明的溶液中:Fe3+、Na+、Cl-、SO42- |
2.某化学研究小组设计如下微型实验探究SO2的化学性质.已知棉球b沾有含酚酞的NaOH溶液.当滴入浓硫酸片刻后发现:棉球a变白,微热后又恢复红色;棉球c变白.以下说法不正确的是( )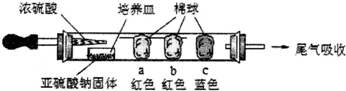

| A. | 本实验是利用强酸制弱酸原理制得SO2气体 | |
| B. | 棉球a沾有品红试液,用以验证SO2的漂白性 | |
| C. | 棉球b红色褪去,说明SO2是酸性氧化物,与水反应能生成亚硫酸 | |
| D. | 棉球C沾有含石蕊的NaOH溶液 |
19.下列各组物质及粒子性质变化不正确的是( )
| A. | 酸性:HClO4>H2SO4>H3AsO4>H3PO4 | |
| B. | 碱性:Ca(OH)2>Mg(OH)2>Al(OH)3 | |
| C. | 金属单质置换出氢的能力:Cs>Rb>K>Ca | |
| D. | 氧化性:F2>Cl2>S |
17.几种短周期元素的原子半径及主要化合价如表:
下列说法正确的是( )
| 元素代号 | X | Y | Z | L | M | Q |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.099 | 0.077 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +7、-1 | +4、-4 | -2 |
| A. | X的最高价氧化物的水化物碱性比Y的弱 | |
| B. | Y既可以和酸反应又可以和碱反应,且化合价变化相同 | |
| C. | 常温下,Z单质可以与L的氢化物溶液反应置换出L单质 | |
| D. | X、M分别与Q形成的化合物中所含化学键类型相同 |
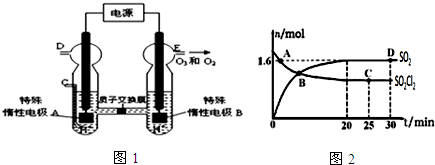
 用化学用语回答下面的问题
用化学用语回答下面的问题