题目内容
8.NH4+的检验:在被检验的溶液中,加入适量的NaOH溶液,并加热,再将一张湿润的红色石蕊试纸放在液面上方,若有变蓝现象,则说明原溶液中有铵根离子存在.分析 检验铵根离子,通常加入强碱溶液加热,然后用湿润的红色石蕊试纸检验,若试纸变蓝,则证明溶液中含有铵根离子,据此进行解答.
解答 解:检验铵根离子的方法为:向待测液里加入NaOH溶液,加热,将湿润的红色石蕊试纸放在液面上方,如果溶液变蓝,则待测液中肯定含有NH4+,
故答案为:NaOH;湿润的红色石蕊试纸;变蓝.
点评 本题考查了常见离子的检验,题目难度不大,明确检验铵根离子的操作方法为解答关键,注意掌握常见离子的性质及检验方法,试题培养了学生的化学实验能力.

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目
18.能用分液漏斗分离的混合物是( )
| A. | 液溴和四氯化碳 | B. | 乙二醇和水 | ||
| C. | NaCl溶液和高级脂肪酸 | D. | 饱和Na2CO3溶液和乙酸乙酯 |
19.下列相关实验不能达到预期目的是( )
| 相关实验 | 预期目的 | |
| ① | 在两份同浓度同体积的H2O2溶液中,分别加2滴FeCl3溶液和2滴CuCl2溶液,前者放在热水中,后者放在冰水中.观察气泡快慢; | 验证温度对化学反应速率的影响. |
| ② | 将氯水加入淀粉KI溶液中 | 验证Cl的非金属性比I强 |
| ③ | 在相同温度下,将表面积相同的铝条和镁条投入等体积同浓度的盐酸中,观察产生气泡的速率. | 比较同周期金属元素的金属性强弱. |
| ④ | 利用电解质溶液的导电性装置,检测AlCl3溶液的导电性 | 证明AlCl3是离子化合物 |
| A. | 仅① | B. | ①④ | C. | ②③ | D. | ③④ |
16.Q、M两元素相邻,M、C、N原子的最外层电子数之和为13,N原子最外层电子数是M原子内层电子数的3倍或者C原子最外层电子数的3倍,M、D原子最外层电子数之和等于C、N原子最外层电子数之和,短周期主族元素Q、M、C、D、N的原子序数依次递增.下列说法正确的是( )
| A. | 元素Q所形成的氧化物只有一种 | |
| B. | 元素M的最高价氧化物对应的水化物为强酸 | |
| C. | 元素C、D、N的最高价氧化物对应的水化物两两之间可发生反应 | |
| D. | 氢化物的稳定性:Q>M |
3.下列有关化学反应速率的说法中正确的是( )
| A. | 100 mL 2 mol•L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气速率不变 | |
| B. | 铁和稀硫酸反应制取氢气时,改用铁片和浓硫酸可加快产生氢气的速率 | |
| C. | 二氧化硫的催化氧化是一个放热反应,所以升高温度,反应速率减慢 | |
| D. | CO和NO可以缓慢反应生成N2和CO2,减小压强,反应速率减慢 |
13.用试纸检验气体性质是一种重要的实验方法.如表所示的实验中(可加热),下列试纸的选用、现象、对应结论都正确的一项是( )
| 序号 | 试剂B | 湿润的试纸A | 结论 |
| A | 碘水 | 淀粉试纸变蓝 | 碘具有氧化性 |
| B | 浓氨水、生石灰 | 蓝色石蕊试纸变红 | 氨气为碱性气体 |
| C | Na2SO3、硫酸 | 品红试纸褪色 | SO2具有漂白性 |
| D | Cu、浓硝酸 | 淀粉KI试纸变蓝 | NO2为酸性气体 |
| A. | A | B. | B | C. | C | D. | D |
11.阿司匹林( 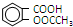 )是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸(
)是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸( 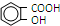 )与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下:
)与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下:
 +(CH3CO)2O$?_{△}^{浓硫酸}$
+(CH3CO)2O$?_{△}^{浓硫酸}$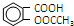 +CH3COOH
+CH3COOH
如图1是工业上制备并提纯阿司匹林的部分流程:
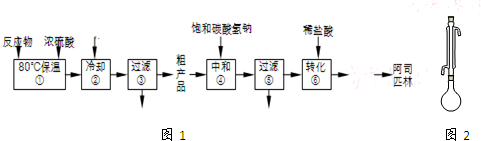
完成下列填空:
(1)步骤①的反应装置如图2所示(加热装置未画出),实验仪器必须干燥的原因是防止乙酸酐与水反应生成乙酸,不利于反应发生;冷凝管的作用是冷凝回流;对烧瓶进行加热的合适方法是水浴加热.
(2)反应中加入的乙酸酐是过量的,过量的目的是提高水杨酸的转化率;步骤②中加入水的目的是使乙酸酐转化为乙酸,同时放出大量的热,需冷却至常温再进行过滤,冷却的目的是减少阿司匹林因溶解而损失(使阿司匹林结晶析出);检验步骤③所得滤液中是否含有水杨酸,可选用的试剂是FeCl3.(写化学式)
(3)步骤④中加入NaHCO3的目的是使阿司匹林转化为易溶于水的盐.
(4)步骤⑤过滤得到的滤渣主要是水杨酸多聚物.步骤⑥中加入盐酸后发生反应的化学方程式为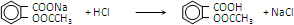 .
.
(5)从步骤⑥到成品纯阿司匹林的剩余操作依次有结晶、过滤、洗涤、干燥.
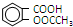 )是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸(
)是世界上应用最广泛的解热、镇痛药.因乙酸很难与酚羟基酯化,工业上以水杨酸( 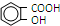 )与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下:
)与乙酸酐[(CH3CO)2O]为主要原料合成阿司匹林.粗产品中主要的副产物是水杨酸多聚物,需进一步提纯.反应原理和相关物理数据如下: +(CH3CO)2O$?_{△}^{浓硫酸}$
+(CH3CO)2O$?_{△}^{浓硫酸}$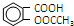 +CH3COOH
+CH3COOH| 名称 | 常温下状态 | 水中溶解性 |
| 乙酸酐 | 液 | 与水反应 |
| 阿司匹林 | 固 | 冷水中微溶;热水中易溶 |
| 水杨酸多聚物 | 固 | 难溶 |

完成下列填空:
(1)步骤①的反应装置如图2所示(加热装置未画出),实验仪器必须干燥的原因是防止乙酸酐与水反应生成乙酸,不利于反应发生;冷凝管的作用是冷凝回流;对烧瓶进行加热的合适方法是水浴加热.
(2)反应中加入的乙酸酐是过量的,过量的目的是提高水杨酸的转化率;步骤②中加入水的目的是使乙酸酐转化为乙酸,同时放出大量的热,需冷却至常温再进行过滤,冷却的目的是减少阿司匹林因溶解而损失(使阿司匹林结晶析出);检验步骤③所得滤液中是否含有水杨酸,可选用的试剂是FeCl3.(写化学式)
(3)步骤④中加入NaHCO3的目的是使阿司匹林转化为易溶于水的盐.
(4)步骤⑤过滤得到的滤渣主要是水杨酸多聚物.步骤⑥中加入盐酸后发生反应的化学方程式为
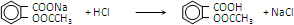 .
.(5)从步骤⑥到成品纯阿司匹林的剩余操作依次有结晶、过滤、洗涤、干燥.

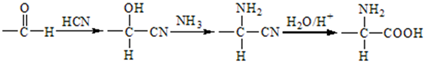
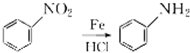
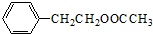 +HNO3(浓)$→_{△}^{浓硫酸}$
+HNO3(浓)$→_{△}^{浓硫酸}$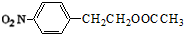 +H2O.
+H2O.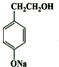 .
.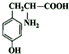 .
.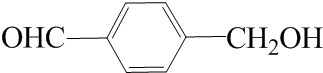 (写结构简式).
(写结构简式).