题目内容
6.密闭容器中的可逆反应:2SO2+O2?2SO3,下列能判断反应达平衡的是①⑦⑧⑨⑩⑪.①在反应的混合物中SO3的量保持不变;
②SO2和O2反应时体积比为2:1;
③SO2、SO3、O2的浓度相等;
④SO2和O2浓度之和等于SO3的浓度;
⑤SO2生成的速度等于SO3消耗的速度;
⑥O2生成的速度等于SO3生成的速度;
⑦O2生成的速度等于SO2消耗速度的$\frac{1}{2}$;
⑧用SO2表示的正反应速率等于用SO3表示的正反应速率;
⑨气体总的物质的量不变;
⑩密闭容器的压强保持不变;
⑪混合气体平均式量保持不变.
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:①在反应的混合物中SO3的量保持不变,反应达到平衡;
②SO2和O2反应时体积比为2:1,不是反应达到平衡状态的标志;
③SO2、SO3、O2的浓度相等,不一定达到平衡;
④SO2和O2浓度之和等于SO3的浓度,不一定达到平衡;
⑤SO2生成的速度等于SO3消耗的速度,反应都是逆反应,不能判断平衡与否;
⑥O2生成的速度等于SO3生成的速度,反应速率不成比例,没有平衡;
⑦O2生成的速度等于SO2消耗速度的$\frac{1}{2}$,正逆反应速率相等,反应达到平衡;
⑧用SO2表示的正反应速率等于用SO3表示的正反应速率,正逆反应速率相等,反应达到平衡;
⑨气体总的物质的量一直在变化,当不变即达平衡;
⑩密闭容器的压强一直在变化,当不变即达平衡;
⑪混合气体平均式量一直在变化,当不变即达平衡;
故答案为:①⑦⑧⑨⑩⑪.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
17.向下列各溶液中通入CO2直到过量,未反生“先产生沉淀,然后沉淀又溶解”这一现象的是( )
①饱和碳酸钠溶液②漂白粉溶液③氯化钙溶液④硅酸钠溶液.
①饱和碳酸钠溶液②漂白粉溶液③氯化钙溶液④硅酸钠溶液.
| A. | ①③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
7.下列关于氯水的叙述,正确的是( )
| A. | 氯水中只含Cl2和HClO两种分子 | |
| B. | 新制氯水只能使蓝色石蕊试纸变红 | |
| C. | 光照氯水有气泡逸出,该气体主要是Cl2 | |
| D. | 氯水放置数天后其pH将变小,酸性增强 |
4.桶烯(Barrelene)的结构简式如图所示,则下列有关说法不正确的是( )
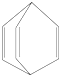

| A. | 桶烯分子中所有原子在同一平面内 | |
| B. | 桶烯在一定条件下能发生加成反应和聚合反应 | |
| C. | 桶烯与苯乙烯(C6H5CH═CH2)互为同分异构体 | |
| D. | 桶烯中的一个氢原子被氯原子取代,所得产物只有一种 |
5.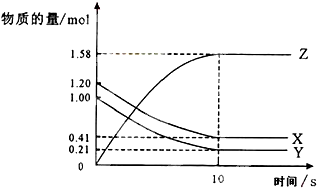 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,下列描述正确的是( )| A. | 反应进行到第10S时,该反应就达到了平衡状态 | |
| B. | 前10S,用Z表示的反应速率为0.158 mol/(L•S) | |
| C. | 反应进行到第8S时,反应速率v(Z)>v(X)>v(Y) | |
| D. | 反应的化学方程式为:X(g)+Y(g)?Z(g) |
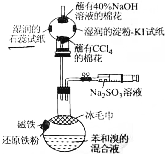 溴苯是一种化工原料,某课外小组用如图装置改进了苯的溴代反应.
溴苯是一种化工原料,某课外小组用如图装置改进了苯的溴代反应.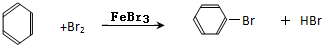 ,冰毛巾覆盖在圆底烧瓶上半部分的目的是降低温度圆底烧瓶上部温度,起冷却回流作用;
,冰毛巾覆盖在圆底烧瓶上半部分的目的是降低温度圆底烧瓶上部温度,起冷却回流作用;