题目内容
17.向下列各溶液中通入CO2直到过量,未反生“先产生沉淀,然后沉淀又溶解”这一现象的是( )①饱和碳酸钠溶液②漂白粉溶液③氯化钙溶液④硅酸钠溶液.
| A. | ①③ | B. | ①③④ | C. | ②③④ | D. | ①②④ |
分析 ①碳酸钠与二氧化碳、水反应生成碳酸氢钠,碳酸氢钠的溶解度小于碳酸钠的溶解度;
②次氯酸钙溶于与二氧化碳反应先生成碳酸钙沉淀,继续通入二氧化碳,二氧化碳与碳酸钙、水反应生成碳酸氢钙;
③盐酸的酸性强于碳酸;
④硅酸钠溶液通入二氧化碳反应生成硅酸沉淀.
解答 解:①向饱和碳酸钠溶液中通入过量的CO2,碳酸钠和二氧化碳、水反应生成碳酸氢钠,碳酸氢钠的溶解性小于碳酸钠的溶解性,原碳酸钠溶液是饱和溶液,生成碳酸氢钠后溶液变成过饱和溶液,所以会析出部分碳酸氢钠晶体,所以不出现“先产生沉淀,然后沉淀又溶解”现象,故选;
②次氯酸钙溶于与二氧化碳反应先生成碳酸钙沉淀,继续通入二氧化碳,二氧化碳与碳酸钙、水反应生成碳酸氢钙,所以会先产生沉淀,然后沉淀又溶解,故不选;
③盐酸酸性强于碳酸,二氧化碳通入氯化钙不反应,故不会发生先产生沉淀,然后沉淀又溶解现象,故选;
④硅酸钠溶液通入二氧化碳反应生成硅酸沉淀,但是硅酸沉淀不会溶解,故选;
故先:B.
点评 本题考查了能发生“先沉淀后溶解”现象的小型综合题,熟悉物质的性质及发生的反应即可解答,注意相关知识的积累.

练习册系列答案
相关题目
7.原子序数依次递增的4种短周期元素可形成简单离子 W2-,X+,Y3+,Z2-,下列说法不正确的是( )
| A. | 工业上常采用电解法冶炼Y 单质 | |
| B. | 气态氢化物的稳定性:H2W强于H2Z | |
| C. | 离子半径由大到小:W2->X+>Y3+>Z2-? | |
| D. | W、X 形成的化合物中阴、阳离子个数比一定是1:2 |
8.钾的还原性比钠强,原因是( )
| A. | K的相对原子质量比较大 | |
| B. | K可失的电子数较多 | |
| C. | K含有的电子数较多 | |
| D. | K和Na最外层电子数相同,但钾原子的半径较大 |
5.下列表述正确的是( )
| A. | 醛基的结构简式-COH | B. | 乙烯的结构简式 C2H4 | ||
| C. | 四氯化碳分子的电子式  | D. | 丙烷分子的球棍模型 |
12.某烃的结构简式为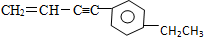 ,下列有关其结构的说法正确的是( )
,下列有关其结构的说法正确的是( )
 ,下列有关其结构的说法正确的是( )
,下列有关其结构的说法正确的是( )| A. | 所有碳原子可能在同一平面上 | B. | 最多有11个碳原子在同一平面上 | ||
| C. | 最多有5个碳原子在同一直线上 | D. | 最多有7个碳原子在同一直线上 |
2.利用下列装置(部分仪器已省略),不能达到实验目的是( )
| A. |  制取少量氨气 | B. |  可制的金属铁 | ||
| C. |  制乙酸乙酯 | D. |  验证混合气体中一定含有乙烯 |
9.取等物质的量的镁粉和铝粉混合,再将混合物平均分为四份,分别加入足量的下列溶液中,充分反应后放出氢气最多的是( )
| A. | 盐酸 | B. | 硝酸 | C. | 氢氧化钠溶液 | D. | 浓硫酸 |
16.下列实验方案合理的是( )
| A. | 将甲烷和乙烯的混合气体通过酸性高锰酸钾溶液,可除去乙烯 | |
| B. | 配制银氨溶液:在一定量AgNO3溶液中,逐滴滴加稀氨水至沉淀恰好溶解为止 | |
| C. | 验证RX为碘代烷,把RX与烧碱水溶液混合加热,将溶液冷却后再加入硝酸银溶液 | |
| D. | 无水乙醇和浓硫酸共热至170℃,将制得的气体通入酸性高锰酸钾可检验制得的气体是否为乙烯 |