题目内容
工业合成氨的反应为N2(g)+3H2(g)?2NH3(g).设t℃在容积为2L的密闭容器中充入0.6mol N2和1.6mol H2,反应在一定条件下达到平衡时,NH3的物质的量分数为
.计算:
(1)达到平衡时H2的物质的量;
(2)t℃该反应的平衡常数.
| 4 |
| 7 |
(1)达到平衡时H2的物质的量;
(2)t℃该反应的平衡常数.
考点:化学平衡的计算
专题:化学平衡专题
分析:(1)先设氮气的转化率为x,利用三段式,计算平衡时生成氨气的物质的量、剩余氮气的物质的量和剩余氢气的物质的量,再结合氨气的质量分数计算氢气的物质的量;
(2)根据平衡常数K=
计算.
(2)根据平衡常数K=
| C2(NH3) |
| C(N2)?C3(H2) |
解答:
解:(1)设氮气的转化率是x,
N2 +3H2 2NH3
2NH3
起始量(mol) 0.6 1.6 0
变化量(mol) 0.6x 1.8x 1.2x
平衡量(mol)0.6(1-x) 1.6-1.8x 1.2x
平衡时,NH3的物质的量分数=
=
,
x=66.7%,所以氢气的物质的量为1.6-1.8x=0.4 mol,
答:达到平衡时H2的物质的量为0.4mol;
(2)平衡时氮气的物质的量浓度=
=0.1mol/L,氢气的物质的量浓度=
=0.2mol/L,氨气的物质的量浓度=
=0.4mol/L,
平衡常数K=
=
=200,
答:该条件下反应的平衡常数为200.
N2 +3H2
 2NH3
2NH3起始量(mol) 0.6 1.6 0
变化量(mol) 0.6x 1.8x 1.2x
平衡量(mol)0.6(1-x) 1.6-1.8x 1.2x
平衡时,NH3的物质的量分数=
| 1.2xmol |
| 0.6(1-x)mol+1.6-1.8x+1.2x |
| 4 |
| 7 |
x=66.7%,所以氢气的物质的量为1.6-1.8x=0.4 mol,
答:达到平衡时H2的物质的量为0.4mol;
(2)平衡时氮气的物质的量浓度=
| 0.2mol |
| 2.0L |
| 0.4mol |
| 2.0L |
| 0.8mol |
| 2.0L |
平衡常数K=
| C2(NH3) |
| C(N2)?C3(H2) |
| (0.4mol/L)2 |
| 0.1mol/L×(0.2mol/L)3 |
答:该条件下反应的平衡常数为200.
点评:本题考查了有关化学平衡的计算,难度不大,注意计算化学平衡常数时各物质的浓度必须是平衡时的浓度.

练习册系列答案
相关题目
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )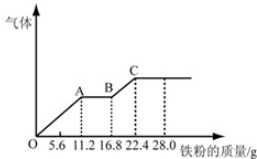

| A、原混合酸中NO3-的物质的量为0.4mol |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为4mol?L-1 |
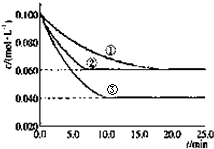 在密闭容器中,反应A(g)+2B(g)?C(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L;c(B)=0.200mol/L;c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )
在密闭容器中,反应A(g)+2B(g)?C(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100mol/L;c(B)=0.200mol/L;c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.下列说法正确的是( )| A、实验②平衡时B的转化率为60% |
| B、反应A(g)+2B(g)?C(g)的△H>0 |
| C、若反应①、②的平衡常数分别为K1、K2,则K1<K2 |
| D、减小反应③的压强,可以使平衡时c(A)=0.060mol/L |
某体积可变的密闭容器,盛有体积比为2:3的N2和H2,在一定条件下发生反应N2(g)+3H2(g)?2NH3(g),若维持温度和压强不变,当达到平衡时,容器的体积为V,其中NH3的体积占20%,下列说法正确的是( )
| A、原混合气体的体积为1.2V |
| B、原混合气体的体积为1.1V |
| C、反应中消耗N2的体积为0.3V |
| D、达到平衡时,消耗H2体积为0.1V |
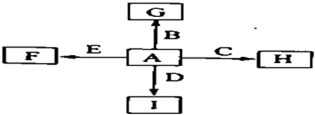 图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知:
图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.已知: