题目内容
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示,下列分析或结果错误的是( )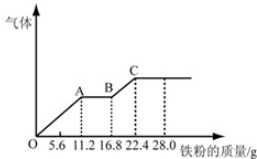

| A、原混合酸中NO3-的物质的量为0.4mol |
| B、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| C、第二份溶液中最终溶质为FeSO4 |
| D、H2SO4浓度为4mol?L-1 |
考点:硝酸的化学性质
专题:氮族元素
分析:由图象可知,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑.
A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,根据铁的物质的量结合离子方程式计算;
B.铁先与硝酸反应生成一氧化氮与铁离子,之后铁与铁离子反应生产亚铁离子,最后是铁和硫酸反应;
C.铁先与硝酸反应,之后铁与铁离子反应生产亚铁离子,最后是铁和硫酸反应,铁单质全部转化为亚铁离子,硝酸全部起氧化剂作用,没有显酸性的硝酸;
D.根据铁和硫酸的反应中铁的质量来确定所需硫酸的量,进而确定硫酸的浓度.
A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,根据铁的物质的量结合离子方程式计算;
B.铁先与硝酸反应生成一氧化氮与铁离子,之后铁与铁离子反应生产亚铁离子,最后是铁和硫酸反应;
C.铁先与硝酸反应,之后铁与铁离子反应生产亚铁离子,最后是铁和硫酸反应,铁单质全部转化为亚铁离子,硝酸全部起氧化剂作用,没有显酸性的硝酸;
D.根据铁和硫酸的反应中铁的质量来确定所需硫酸的量,进而确定硫酸的浓度.
解答:
解:A.OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,硝酸全部起氧化剂作用,所以n(NO3-)=n(Fe)=
=0.2mol,故A错误;
B、由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,故B正确;
C、硝酸全部被还原,没有显酸性的硝酸,因为溶液中有硫酸根,并且铁单质全部转化为亚铁离子,所以溶液中最终溶质为FeSO4,故C正确;
D、反应消耗22.4g铁,也就是
=0.4mol,所有的铁都在硫酸亚铁中,根据硫酸根守恒,所以每份含硫酸0.4mol,所以硫酸的浓度是
=4mol/L,故D正确,
故选A.
| 11.2g |
| 56g/mol |
B、由图象可知,由于铁过量,OA段发生反应为:Fe+NO3-+4H+=Fe3++NO↑+2H2O,AB段发生反应为:Fe+2Fe3+=3Fe2+,BC段发生反应为:Fe+2H+=Fe2++H2↑,故B正确;
C、硝酸全部被还原,没有显酸性的硝酸,因为溶液中有硫酸根,并且铁单质全部转化为亚铁离子,所以溶液中最终溶质为FeSO4,故C正确;
D、反应消耗22.4g铁,也就是
| 22.4 |
| 56 |
| 0.4 |
| 0.1 |
故选A.
点评:本题以图象为载体,考查有关金属和酸反应的计算题,难度较大,关键根据图象分析各段发生的反应,注意与铁的反应中硝酸全部起氧化剂作用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列表达正确的是( )
| A、常温下,用0.1mol?L-1 NaOH溶液滴定10.00mol?L-1 CH3COOH溶液,在滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
| B、等物质的量Na2S和NaHS混合溶液中c(OH-)=c(H+)+2c(H2S)+c(HS-) |
| C、x mol Cl2溶于水得到1L溶液,则c(Cl-)+c(HClO)=2x mol?L-1 |
| D、常温下,0.1mol?L-1的下列溶液:①NH4Al(SO4)2;②NH4Cl;③NH3?H2O;④CH3COONH4,c(NH4+)由大到小的顺序是:②>①>④>③ |
PbO2是褐色固体,受热分解为Pb的+4和+2价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3:2,则剩余固体的组成及物质的量比是( )
| A、1:2混合的PbO2、Pb3O4 |
| B、1:1混合的Pb3O4、PbO |
| C、1:4:1混合的PbO2、Pb3O4、PbO |
| D、4:1:1混合的PbO2、Pb3O4、PbO |
设NA为阿伏加德罗常数的值,下列说法全部错误的组合是( )
a 12g金刚石中含有的碳碳键的数目为2NA
b 1mol明矾与水完全反应转化为氢氧化铝胶体后,其中胶体粒子的数目为NA
c 标准状况下,2.24L乙烯和丙烯等物质的量混合气体中含有的共用电子对的数目为0.75NA
d 常温下,1mol?L-1的NH4NO3溶液中含有氮原子的数目为2NA
e 标准状况下,2.24L C6H14含原子总数大于2NA
f 17g H2O2中含有的电子数为9NA
g 将2mol SO2与1mol O2混合,发生反应转移的电子总数一定是4NA
h 常温下100mL 1mol?L-1 AlCl3溶液中阳离子总数大于0.1NA.
a 12g金刚石中含有的碳碳键的数目为2NA
b 1mol明矾与水完全反应转化为氢氧化铝胶体后,其中胶体粒子的数目为NA
c 标准状况下,2.24L乙烯和丙烯等物质的量混合气体中含有的共用电子对的数目为0.75NA
d 常温下,1mol?L-1的NH4NO3溶液中含有氮原子的数目为2NA
e 标准状况下,2.24L C6H14含原子总数大于2NA
f 17g H2O2中含有的电子数为9NA
g 将2mol SO2与1mol O2混合,发生反应转移的电子总数一定是4NA
h 常温下100mL 1mol?L-1 AlCl3溶液中阳离子总数大于0.1NA.
| A、a c f h |
| B、a c e g |
| C、a c e f h |
| D、b d g |
 由短周期元素组成的常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去).若( )
由短周期元素组成的常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去).若( )| A、X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应 |
| B、A是单质,B和D的反应是OH-+HCO3-→H2O+CO32-,则E一定能还原Fe2O3 |
| C、X是O2,且C与D摩尔质量相差16,则A一定为Mg3N2 |
| D、D为白色沉淀,与A摩尔质量相等,则X一定是铝盐 |
某阳离子与Ar具有相同的电子层结构,阴离子与Ne具有相同的电子层结构,该阴、阳离子所形成的化合物可能是( )
| A、K2S |
| B、NaF |
| C、CaF2 |
| D、Na2O |
下列离子方程式正确的是( )
| A、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O |
| B、Fe3O4溶液稀盐酸:Fe3O4+8H+═3Fe3++4H2O |
| C、用烧碱溶液吸收氯气:Cl2+2OH-═Cl-+ClO-+H2O |
| D、向硫酸亚铁溶液中加入用硫酸酸化的H2O2溶液Fe2++H2O2+2H+═Fe3++4H2O |
下列有机物命名正确的是( )
| A、1,3,4-三甲苯 |
| B、2-甲基丙烷 |
| C、1-甲基-1-丙醇 |
| D、2-甲基-3-丁炔 |