题目内容
【题目】亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO和Cl2反应得到,化学方程式为2NO(g)+Cl2(g) ![]() 2NOCl(g)。
2NOCl(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
①2NO2(g)+NaCl(s) ![]() NaNO3(s)+NOCl(g)
NaNO3(s)+NOCl(g)
②4NO2(g)+2NaCl(s) ![]() 2NaNO3(s)+2NO(g)+Cl2(g)
2NaNO3(s)+2NO(g)+Cl2(g)
③2NO(g)+Cl2(g) ![]() 2NOCl(g)
2NOCl(g)
设反应①②③对应的平衡常数依次为K1、K2、K3,则K1、K2、K3之间的关系为____________。
(2)300 ℃时,2NOCl(g) ![]() 2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为速率常数,只与温度有关),测得速率与浓度的关系如表所示:
2NO(g)+Cl2(g)。正反应速率的表达式为v正=k·cn(NOCl)(k为速率常数,只与温度有关),测得速率与浓度的关系如表所示:
序号 | c(NOCl)/mol·L-1 | v/mol·L-1·s-1 |
① | 0.30 | 3.60×10-9 |
② | 0.60 | 1.44×10-8 |
③ | 0.90 | 3.24×10-8 |
n=________,k=________。
(3)在1 L恒容密闭容器中充入2 mol NO(g)和1 mol Cl2(g),在不同温度下测得c(NOCl)与时间t的关系如图A所示:反应开始到10 min时Cl2的平均反应速率v(Cl2)=________ mol·L-1·min-1。
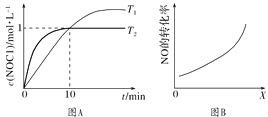
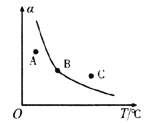
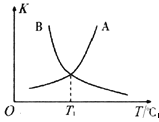
(4)在密闭容器中充入NO(g)和Cl2(g),改变外界条件[温度、压强、![]() 、与催化剂的接触面积],NO的转化率变化关系如图B所示。X代表________。
、与催化剂的接触面积],NO的转化率变化关系如图B所示。X代表________。
【答案】 K2·K3=K 2 4.0×10-8 L· mol-1·s-1 0.05 压强或![]()
【解析】本题主要考查化学平衡的影响因素及反应速率的计算。
(1)2①=②+③对应的平衡常数依次为K1、K2、K3,则K1、K2、K3之间的关系为K2·K3=K。
(2) 速率与浓度的平方成正比,所以n=2,代入一组数值得k=4.0×10-8 L· mol-1·s-1。
(3)v(Cl2)=1/2/10 mol·L-1·min-1=0.05 mol·L-1·min-1。
(4)NO的转化率随着X增大而增大。该反应放热,温度升高平衡左移,NO的转化率减小。该反应气体物质的量减小,增大压强平衡右移,NO的转化率增大。![]() 增大,NO的转化率增大。与催化剂的接触面积增大,反应速率增大,NO的转化率不变。因此,X代表压强或
增大,NO的转化率增大。与催化剂的接触面积增大,反应速率增大,NO的转化率不变。因此,X代表压强或![]() 。
。