题目内容
20.下列相关实验的操作或结论正确的是( )| A. | 将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯 | |
| B. | 制硝基苯时温度计水银球在反应液中 | |
| C. | 实验室制乙烯时温度计水银球在反应液中 | |
| D. | 检验溴乙烷中的溴元素时,将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,滴加AgNO3溶液 |
分析 A.二氧化硫也可使溴水褪色;
B.制备硝基苯是在50℃-60℃温度下水浴加热;
C.实验室制乙烯时,需要测定反应液温度,必须将温度计的水银球插入反应液中;
D.冷却后的溶液为碱性,需要加入硝酸中和后再滴加硝酸银,否则干扰溴离子的检验.
解答 解:A.二氧化硫也可使溴水褪色,则将某气体通入溴水中,溴水颜色褪去,该气体不一定是乙烯,故A错误;
B.硝基苯的制取反应需要水浴加热,因而要测定水浴的温度,故B错误;
C.实验室制乙烯时,需要测定反应液温度,必须将温度计的水银球插入反应液中,故C正确;
D.将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgNO3溶液,故D错误;
故选C.
点评 本题考查有机物的鉴别、化学实验基本操作方法判断等知识,题目难度中等,试题综合性较强,侧重有机物性质及性质实验的考查,把握发生的反应及反应中的现象、实验细节等为解答的关键,选项D为易错点,注意掌握正确的操作方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.N、Cu、H、O、S、Mg是常见的六种元素:
(1)Mg位于元素周期表第三周期第IIA族;N与O的基态原子核外未成对电子个数比为
3:2;Cu的基态原子电子排布式为1s22s22p63s23p63d104s1.
(2)用“>”或“<”填空:
(3)Mg在空气中燃烧可微量生产氮化镁(Mg3N2),Mg3N2(S)溶于足量的稀硫酸可得到两种正盐,在25℃、101kPa下,已知该反应每消耗1mol H2SO4放热akJ,则该反应的热化学方程式为Mg3N2(S)+4H2SO4(aq)=3MgSO4(aq)+(NH4)2SO4(aq)△H=-4akJ/mol.
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽).写出该反应的化学方程式,并标出电子转移的方向和数目 .
.
(1)Mg位于元素周期表第三周期第IIA族;N与O的基态原子核外未成对电子个数比为
3:2;Cu的基态原子电子排布式为1s22s22p63s23p63d104s1.
(2)用“>”或“<”填空:
| 碱性: Mg (OH)2> Cu(OH)2 | 第一电离能:O< N | 熔点: MgS< MgO | 稳定性: H2S< H2O |
(4)工业上采取加热条件下用氨气还原氧化铜制取铜,同时得到两种无污染的气体(或蒸汽).写出该反应的化学方程式,并标出电子转移的方向和数目
 .
.
15.下列说法错误的是( )
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | 相对分子质量相等的两种物质,不一定是同分异构体 | |
| D. | 烯烃各同系物含碳的质量分数相等 |
9.X、Y、Z、R分别代表四种元素,若aXm+、bYn+、cZn-、dRm-四种离子的核外电子排布相同,且m>n,则下列关系正确的是( )
| A. | a-c=m-n | B. | b+d=m+n | C. | a>b>d>c | D. | a>b>c>d |
10.A、B、C、D四种非金属元素,A、B在反应中各结合1个电子形成稳定结构,放出能量B<A;氢化物稳定性HD>HA;原子序数C<B,其稳定结构的核外电子数相等.则四种元素非金属性由强到弱的顺序正确的是( )
| A. | A、B、C、D | B. | B、A、C、D | C. | D、A、B、C | D. | B、A、D、C |
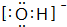
 (1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在
(1)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料.已知在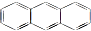 与苯炔(
与苯炔(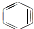 )反应生成化合物X(立体对称图形),如图所示:
)反应生成化合物X(立体对称图形),如图所示: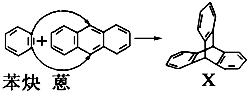
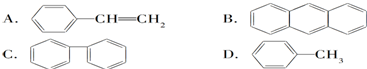
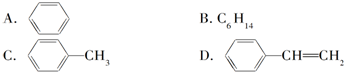
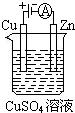
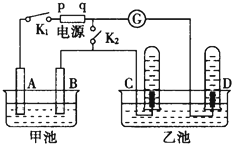 在如图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,立即停止电解,取出A电极,洗涤、干燥、称量,电极质量增重1.6g.请回答下列问题:
在如图均用石墨作电极的电解池中,甲池中为500mL含某一溶质的蓝色溶液,乙池中为500mL稀硫酸,闭合K1,断开K2进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,立即停止电解,取出A电极,洗涤、干燥、称量,电极质量增重1.6g.请回答下列问题: