题目内容
15.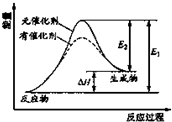 某反应的过程中能量辩护如图实数(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列叙述制取的是( )
某反应的过程中能量辩护如图实数(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列叙述制取的是( )| A. | 该反应为放热反应 | |
| B. | 催化解能改变反应的焓变 | |
| C. | 催化解能降低反应所需活化能,增大活化分子百分数 | |
| D. | 逆反应的活化能大于正反应的活化能 |
分析 A、吸热反应中,生成物的总能量高;
B、催化剂只改变速率不改变反应物和生成物的能量;
C、催化剂改变化学反应速率是降低了反应的活化能;
D、图象中E1大.
解答 解:A、图象中反应物能量低于生成物能量,故反应是吸热反应,故A错误;
B、反应的焓变取决于反应物和生成物的总能量的高低,而催化剂不能改变反应物和生成物所具有的能量,故不能改变该反应的焓变,只能改变反应速率,故B错误;
C、催化剂只所以能加快化学反应速率是因为催化剂的使用降低了反应的活化能,提高了活化分子百分数,故C正确;
D、图象可知逆反应的活化能E2小于正反应的活化能E1,故D错误;
故选C.
点评 本题考查了化学反应的能量变化分析,催化剂的作用实质,图象识别和理解含义是解题关键.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
5.下列有关同分异构体数目的叙述中,正确的是( )
| A. | C5H12有2种同分异构体 | |
| B. | 甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得物质共有6种 | |
| C. | C8H10中只有三种属于芳香烃的同分异构体 | |
| D. | CH3CH2CH2CH3光照下与氯气反应,只生成一种一氯代烃 |
6.下列叙述正确的是( )
| A. | 20g重水(D2O)含有的电子数为10 NA | |
| B. | 46g NO2和N2O4的混合物中所含氧原子个数为6.02×1023 | |
| C. | 0.1mol过氧化钠与足量的水反应,转移的电子数为 0.2NA | |
| D. | 1L 0.3 mol/LNa2SO4溶液中,含有Na+和SO42-总数为0.6 NA |
3. 氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
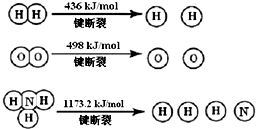
(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同.已知:
2H2(g)+O2(g)=2H2O (g)△H=-483.6kJ/mol
3H2 (g)+N2(g) 2NH3(g)△H=-92.4kJ/mol
计算断裂1mol N≡N键需要能量946kJ,氮气分子中化学键比氧气分子中的化学键键强(填“强”或“弱”),因此氢气与二者反应的条件不同.
(2)固氮是科学家致力研究的重要课题.自然界中存在天然的大气固氮过程:N2(g)+O2(g)=2NO (g)△H=+180.8kJ/mol,工业合成氨则是人工固氮.分析两种固氮反应的平衡常数,下列结论正确的是BC.
A.常温下,大气固氮几乎不可能进行,而工业固氮非常容易进行
B.人类大规模模拟大气固氮是无意义的
C.工业固氮温度越低,氮气与氢气反应越完全
D.K越大说明合成氨反应的速率越大.
 氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究
氨气是生产化肥、硝酸等的重要原料,围绕合成氨人们进行了一系列的研究(1)氢气既能与氮气又能与氧气发生反应,但是反应的条件却不相同.已知:
2H2(g)+O2(g)=2H2O (g)△H=-483.6kJ/mol
3H2 (g)+N2(g) 2NH3(g)△H=-92.4kJ/mol
计算断裂1mol N≡N键需要能量946kJ,氮气分子中化学键比氧气分子中的化学键键强(填“强”或“弱”),因此氢气与二者反应的条件不同.
(2)固氮是科学家致力研究的重要课题.自然界中存在天然的大气固氮过程:N2(g)+O2(g)=2NO (g)△H=+180.8kJ/mol,工业合成氨则是人工固氮.分析两种固氮反应的平衡常数,下列结论正确的是BC.
| 反应 | 大气固氮 | 工业固氮 | ||||
| 温度/℃ | 27 | 2000 | 25 | 350 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.847 | 0.507 | 0.152 |
B.人类大规模模拟大气固氮是无意义的
C.工业固氮温度越低,氮气与氢气反应越完全
D.K越大说明合成氨反应的速率越大.
10.已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上常温下呈气态的化合物,则下列说法错误的是( )
| A. | X、Y、Z三种元素可以组成一种盐 | |
| B. | Y和Z可以组成一种Y和Z的质量比为7:8的化合物 | |
| C. | 由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒都有2种 | |
| D. | X和Z可以组成原子个数比分别为1:1和2:1常温下为液态的两种化合物 |
20.下列仪器的使用或操作正确的是( )
| A. | 分液漏斗中液体的总体积不得超过其容量的2/3 | |
| B. | 萃取时,用右手压住分液漏斗的玻璃塞,左手握住旋塞,将分液漏斗倒过来用力震荡 | |
| C. | 分液漏斗的检漏只需检查旋塞处是否漏水即可 | |
| D. | 课本中测定中和热实验的装置,用铜制环形搅棒代替玻璃环形搅棒更耐用 |
4.将铜粉放入稀硫酸中,加热无明显反应发生.但加入某物质后,发现铜粉质量逐渐减少,该物质不可能是( )
| A. | Fe2(SO4)3 | B. | ZnSO4 | C. | KNO3 | D. | O2 |
5.下列各组溶液中,不用任何试剂无法鉴别的是( )
| A. | NaCl、Na2CO3、NaI、AgNO3 | B. | HCl、Na2CO3、新制氯水、NaI | ||
| C. | Na2S、HCl、FeCl3、NaCl | D. | AlCl3、BaCl2、Na2CO3、H2SO4 |