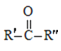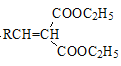题目内容
【题目】氢、碳和氯的单质及化合物在生产和生活中有广泛用途。
(1)H2(g)+Cl2 (g) =2HCl(g) ΔH反应的能量变化示意图如图1所示,其中436kJ/mol表示的含义是_____,由图计算ΔH=____kJ/mol。
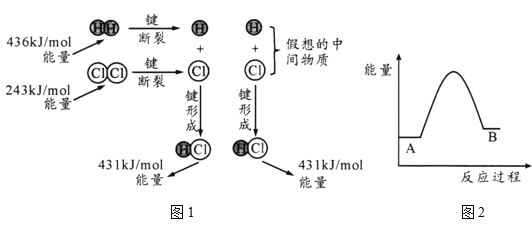
(2)金刚石、石墨的燃烧热分别为395.4kJ/mol和393.5kJ/mol。图2是两者相互转化的能量变化示意图,A表示的物质为_____。
【答案】1molH2分子中的化学键断裂时需要吸收的最少能量(或H-H键的键能) -183 石墨
【解析】
(1)根据图示,436kJ/mol是H-H键的键能;结合ΔH=反应物的键能之和-生成物的键能之和计算;
(2)根据金刚石、石墨的燃烧热判断金刚石和石墨能量的相对大小再结合图像分析判断。
(1)根据图示,436kJ/mol表示1molH2分子中的化学键断裂时需要吸收的能量(或H-H键的键能);ΔH=反应物的键能之和-生成物的键能之和,则H2(g)+Cl2 (g) =2HCl(g) ΔH=(436kJ/mol+243kJ/mol)-2×431kJ/mol=-183 kJ/mol,故答案为:1molH2分子中的化学键断裂时需要吸收的最少能量(或H-H键的键能);-183;
(2)金刚石、石墨的燃烧热分别为395.4kJ/mol和393.5kJ/mol,说明金刚石的能量较高,因此能量较低的A表示石墨,故答案为:石墨。

【题目】硝酸亚铁可用作媒染剂、分析试剂、催化剂等。
(1)硝酸亚铁可用铁屑在低温下溶于稀硝酸制得,还原产物为NO。反应的化学方程式为________。
(2)某小组为探究硝酸亚铁晶体的热分解产物,按下图所示装置进行实验。
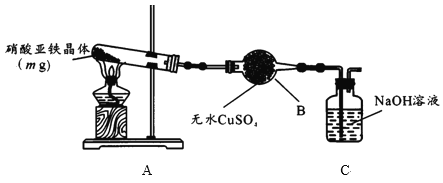
①仪器B的名称是____,实验中无水CuSO4变蓝,由此可知硝酸亚铁晶体含有___。
②实验中观察到A装置的试管中有红棕色气体生成,检验热分解后固体为氧化铁的实验方案为:
实验步骤 | 现象 |
取少量固体加适量稀硫酸,振荡,将溶液分成两份 | 固体溶解得黄色溶液 |
一份滴入____ | 溶液变成红色 |
另一份滴入1~2滴K3 [Fe(CN)6]溶液 | ___________ |
A中硝酸亚铁晶体[Fe(NO3)2·xH2O]分解的化学方程式为______ 。
(3)继续探究mg硝酸亚铁晶体中铁元素的质量分数
①取A中热分解后的固体放入锥形瓶,用稀硫酸溶解,加入过量的KI溶液,滴入2滴___作指示剂。
②用a mol/LNa2S2O3标准溶液滴定锥形瓶中的溶液(已知:I2+2S2O32-=2I-+S4O62-),滴定至终点时用去bmLNa2S2O3溶液,则硝酸亚铁晶体中铁的质量分数为______。