题目内容
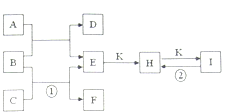
【题目】如图是常见的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,C为活泼的金属单质,B是最常见的无色液体,A是单质C在D中燃烧生成的淡黄色固体,I是焙制糕点所用的发酵粉的主要成分之一(反应中生成的部分物质已略去)。
(1)K的分子式为___。
(2)物质A的常见用途为________(任写一种即可)。
(3)反应①的化学方程式为______。
反应②的化学方程式为_______。
【答案】CO2 漂白剂或供氧剂 2Na+2H2O===2NaOH+H2↑ 2NaHCO3![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
【解析】
A是由单质C在D中燃烧生成的淡黄色固体,淡黄色固体为Na2O2,则A为Na,C为O2,D为Na2O2,I是焙制糕点所用的发酵粉的主要成分之一,应为NaHCO3,B是最常见的无色液体,应为H2O,则E为NaOH,F为H2,K为CO2,H为Na2CO3。
(1)由以上分析可知K为CO2,故答案为:CO2。
(2)A为Na2O2,具有漂白性、氧化性,可与水或CO2反应生成O2,可用于供氧剂,故答案为:漂白剂或供氧剂。
(3)反应①为Na和水的反应,反应方程式为2Na+2H2O===2NaOH+H2↑,NaHCO3不稳定,加热可分解生成Na2CO3和CO2,反应方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑,故答案为:2Na+2H2O===2NaOH+H2↑;2NaHCO3
Na2CO3+H2O+CO2↑,故答案为:2Na+2H2O===2NaOH+H2↑;2NaHCO3![]() Na2CO3+H2O+CO2↑。
Na2CO3+H2O+CO2↑。

 阅读快车系列答案
阅读快车系列答案【题目】一定温度下,在三个体积均为0.5 L的恒容密闭容器中发生反应:CO(g)+Cl2(g)![]() COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
COCl2(g),其中容器Ⅰ中反应在5 min时达到平衡状态。
容器编号 | 温度/℃ | 起始物质的量/mol | 平衡物质的量/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
Ⅰ | 500 | 1.0 | 1.0 | 0 | 0.8 |
Ⅱ | 500 | 1.0 | a | 0 | 0.5 |
Ⅲ | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
下列说法中正确的是
A. 容器Ⅰ中前5 min的平均反应速率v(CO)=0.16 mol·L-1·min-1
B. 该反应正反应为吸热反应
C. 容器Ⅱ中起始时Cl2的物质的量为0.55 mol
D. 若起始时向容器Ⅰ加入CO0.8mol、Cl20.8mol,达到平衡时CO转化率大于80%