题目内容
15.下列实验方案设计中,可行的是( )| A. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 | |
| B. | 用萃取的方法分离汽油和煤油 | |
| C. | 将稀H2SO4与BaCl2的反应设计成原电池 | |
| D. | 将氢气和氧气的混合气体通过灼热的氧化铜,以除去其中的氢气 |
分析 A.Mg、Al均与盐酸反应,而Cu不能;
B.汽油和煤油互溶,但沸点不同;
C.稀H2SO4与BaCl2的反应为非氧化还原反应;
D.氢气和氧气的混合气体加热可能发生爆炸,且氢气还原CuO可生成水蒸气.
解答 解:A.Mg、Al均与盐酸反应,而Cu不能,则加稀盐酸后过滤,可除去混在铜粉中的少量镁粉和铝粉,故A正确;
B.汽油和煤油互溶,但沸点不同,则不能利用萃取分离,应选蒸馏分离,故B错误;
C.稀H2SO4与BaCl2的反应为非氧化还原反应,只有放热的氧化还原反应可设计为原电池,故C错误;
D.氢气和氧气的混合气体加热可能发生爆炸,且氢气还原CuO可生成水蒸气,混有新杂质,则不能除杂,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、原电池等,把握物质的性质、反应原理等为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
5.下列各组物质形成的晶体中,晶体类型相同的是( )
| A. | 晶体硅和SiC | B. | C60和Mg | C. | NaCl和HCl | D. | SO2和SiO2 |
6.下列说法正确的是( )
| A. | 两种化合物组成元素相同,且各元素的质量分数也相同,则两者一定是同分异构体 | |
| B. | 分子中有6个碳原子的烃只能形成5个碳碳单键 | |
| C. | 丙烯分子中的所有原子都在同一平面内 | |
| D. | 分子式为C3H6Cl2与C3H2Cl6的有机物所具有的同分异构体数目相同 |
3.把1OOmL2mol/L的H2SO4跟过量锌粉反应.在一定温度下,为了减缓反应速率而不影响生成H2的总量,可在反应物中加入适量的( )
| A. | 醋酸钠溶液 | B. | 硫酸铜溶液 | C. | 硝酸钠溶液 | D. | 氢氧化钠溶液 |
7.据碘与氢气反应的热化学方程式
(1)I2(g)+H2(g)?2HI(g)△H=-9.48 kJ•mol-1
(2)I2(s)+H2(g)?2HI(g)△H=+26.48 kJ•mol-1
下列判断正确的是( )
(1)I2(g)+H2(g)?2HI(g)△H=-9.48 kJ•mol-1
(2)I2(s)+H2(g)?2HI(g)△H=+26.48 kJ•mol-1
下列判断正确的是( )
| A. | 254gI2( g)中通入 2gH2( g),反应放热 9.48 kJ | |
| B. | 1mol固态碘与1mol气态碘所含的能量相差17.00kJ | |
| C. | 反应(1)的产物比反应(2)的产物稳定 | |
| D. | 反应(2)的反应物总能量比反应(1)的反应物总能量低 |
5.下列有关离子方程式与所述事实相符的是( )
| A. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | |
| B. | 某溶液中存在大量Fe3+、S2-、Cl-、Na+,加入NaOH溶液发生反应:Fe3++3OH-=Fe(OH)3↓ | |
| C. | 向AlCl3溶液中投入过量的Na:Na+Al3++2H2O=Na++AlO2-+2H2↑ | |
| D. | 将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑ |
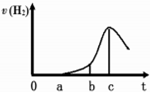 某兴趣小组进行“活泼金属与酸反应”的实验.将5.4g的铝片投入500mL0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图.
某兴趣小组进行“活泼金属与酸反应”的实验.将5.4g的铝片投入500mL0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图.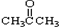 ③CH3CH2Br ④
③CH3CH2Br ④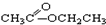 ⑤
⑤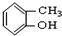 ⑥
⑥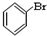 ⑦
⑦ ⑧
⑧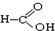 ⑨
⑨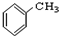 ⑩
⑩