题目内容
5.下列有关离子方程式与所述事实相符的是( )| A. | 用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | |
| B. | 某溶液中存在大量Fe3+、S2-、Cl-、Na+,加入NaOH溶液发生反应:Fe3++3OH-=Fe(OH)3↓ | |
| C. | 向AlCl3溶液中投入过量的Na:Na+Al3++2H2O=Na++AlO2-+2H2↑ | |
| D. | 将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑ |
分析 A.发生氧化还原反应生成碘、水;
B.Fe3+、S2-发生氧化还原反应;
C.投入过量的Na,反应生成偏铝酸钠、氯化钠和水,电子、电荷不守恒;
D.过氧化钠为氧化剂也为还原剂.
解答 解:A.用过氧化氢从酸化的海带灰浸出液中提取碘的离子反应为2I-+H2O2+2H+═I2+2H2O,故A正确;
B.Fe3+、S2-发生氧化还原反应,不能大量共存,故B错误;
C.向AlCl3溶液中投入过量的Na的离子反应为4Na+Al3++2H2O=4Na++AlO2-+2H2↑,故C错误;
D.将Na2O2固体投入H218O中的离子反应为2H218O+2Na2O2=2OH-+218OH-+4Na++O2↑,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应的离子反应考查,注意电子、电荷守恒的分析,题目难度不大.

练习册系列答案
相关题目
15.下列实验方案设计中,可行的是( )
| A. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 | |
| B. | 用萃取的方法分离汽油和煤油 | |
| C. | 将稀H2SO4与BaCl2的反应设计成原电池 | |
| D. | 将氢气和氧气的混合气体通过灼热的氧化铜,以除去其中的氢气 |
10.W、X、Y、Z为原子序数递增的四种短周期元素.W是原子半径最小的元素,X的一种核素在考古时常用来鉴定一些文物的年代,Y是植物生长所需化学肥料中主要的营养元素之一,Z原子的最外层电子数是X原子最外层电子数的1.5倍.下列说法正确的是( )
| A. | 氢化物的沸点:Z一定高于Y | |
| B. | 最高价氧化物对应水化物的酸性:X强于Y | |
| C. | W、X、Y、Z都能分别与氯元素形成共价化合物 | |
| D. | 仅由W、Y、Z三种元素组成的化合物不可能属于盐类 |
14.已知阴离子R2-的原子核内有n个中子,R原子的质量数为m,则w gR2-所含有电子的物质的量是( )
| A. | $\frac{m-n-2}{w•m}$ mol | B. | $\frac{w?m-n?}{n}$mol | C. | $\frac{w}{m}$(m-n-2)mol | D. | $\frac{w}{m}$(m-n+2)mol |
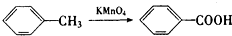

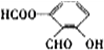 、
、 、
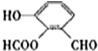
、
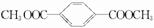 .
.