题目内容
1.下列说法不正确的是( )| A. | 离子化合物中可以含有共价键,但共价化合物中一定不含离子键 | |
| B. | 气态单质分子中一定存在共价键 | |
| C. | 氢元素即可与氯元素形成共价键也可与钠元素形成离子键 | |
| D. | 金属元素和非金属元素形成的化合物不一定是离子化合物 |
分析 A.离子化合物中一定含有离子键,可能含有共价键,只含共价键的化合物是共价化合物;
B.气态单质分子中不一定存在共价键;
C.活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键;
D.金属元素和非金属元素形成的化合物不一定是离子化合物,可能是共价化合物.
解答 解:A.离子化合物中一定含有离子键,可能含有共价键,如KOH,只含共价键的化合物是共价化合物,故A正确;
B.气态单质分子中不一定存在共价键,如稀有气体,故B错误;
C.活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,所以氢元素即可与氯元素形成共价键也可与钠元素形成离子键,故C正确;
D.金属元素和非金属元素形成的化合物不一定是离子化合物,可能是共价化合物,如氯化铝,故D正确;
故选B.
点评 本题考查化学键和物质的关系,明确物质构成微粒及微粒之间作用力是解本题关键,易错选项是BD,注意不能根据是否含有金属元素判断离子键,稀有气体中不存在化学键,只存在分子间作用力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列递变规律正确的是( )
| A. | HClO4、H2SO4、H3PO4的酸性依次增强 | |
| B. | P、S、Cl最高正价依次降低 | |
| C. | HCl、HBr、HI的稳定性依次增强 | |
| D. | 钠、镁、铝的金属性依次减弱 |
12.X、Y、Z、W、M均为短周期元素且原子序数依次增大,X、M同主族;Z+、W3+与Y2-具有相同的电子层结构;M 是地壳中含量占第二的元素.下列说法正确的是( )
| A. | 原子最外层电子数:X>Y>Z | B. | 粒子半径:r(W3+)>r(Y2-)>r(Z+) | ||
| C. | MY2与Z2Y的化合物类型相同 | D. | 单质沸点:M>Z>Y |
10.下列关于油脂的叙述不正确的是( )
| A. | 油脂属于脂类 | B. | 油脂都不能使溴水褪色 | ||
| C. | 油脂没有固定的熔沸点 | D. | 油脂是高级脂肪酸的甘油酯 |
1.在101kPa 25℃时,1.0g乙烷气体完全燃烧生成液态水时放出热量52.0kJ,则乙烷燃烧的热化学方程式为( )
| A. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-1560kJ•mol-1 | |
| B. | 2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=-1560kJ•mol-1 | |
| C. | 2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=+3120 kJ•mol-1 | |
| D. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-52.0kJ•mol-1 |




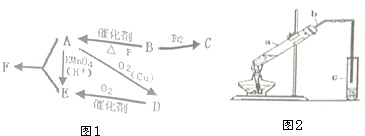 有机物A仅由C、H、O三种元素组成,一定条件下A、B、C、D、E、F之间的转化如图1所示,已知B的产量是衡量一个国家石油化工发展水平的标志.回答下列问题:
有机物A仅由C、H、O三种元素组成,一定条件下A、B、C、D、E、F之间的转化如图1所示,已知B的产量是衡量一个国家石油化工发展水平的标志.回答下列问题: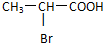 ;
;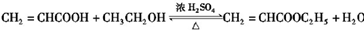 ,该反应的反应类型为酯化反应(或取代反应);
,该反应的反应类型为酯化反应(或取代反应);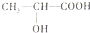 ,试写出C与金属Na反应的化学方程式为:
,试写出C与金属Na反应的化学方程式为: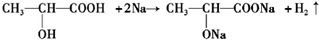 .
. 2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.请回答下列问题.
2SO2(g)+O2(g)=2SO3(g)反应过程的能量变化如图所示.请回答下列问题.