题目内容
【题目】(1)在25℃、101kPa下,一定质量的无水乙醇完全燃烧时放出热量Q kJ,其燃烧生成的CO2用过量饱和石灰水吸收可得100gCaCO3沉淀,则乙醇燃烧的热化学方程式为___。
(2)已知下列热化学方程式
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1= -25kJ·mol-1 ①
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2= -47kJ·mol-1 ②
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3= +19kJ·mol-1 ③写出FeO(s)被CO还原成Fe和CO2的热化学方程式____。
(3)向足量H2SO4溶液中加入100mL 0.4mol·L-1Ba(OH)2溶液,放出的热量是5.12kJ。如果向足量Ba(OH)2溶液中加入100mL 0.4mol·L-1盐酸时,放出的热量为2.2kJ。则Na2SO4溶液与BaCl2溶液反应的热化学方程式为___。
【答案】C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH= -2Q kJ/mol FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH= -11kJ·mol-1 Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH= -18kJ·mol-1
【解析】
(1)因生成的CO2用过量饱和石灰水完全吸收,可得100g CaCO3沉淀,CaCO3的物质的量是1mol,由碳元素守恒可知,二氧化碳的物质的量也为1mol,即生成1mol二氧化碳放出的热量为Q,而完全燃烧1mol无水乙醇时生成2mol二氧化碳,则放出的热量为Q×2=2Q,热化学方程式为:C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH= -2Q kJ/mol;
(2)①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g);ΔH= -25kJ/mol,
②3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g);ΔH= -47kJ/mol,③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g);ΔH= +19kJ/mol,
依据盖斯定律①×3-(③×2+②)得到:6CO(g)+6FeO(s)=6Fe(g)+6CO2(g) ΔH= -66kJ/mol;得到热化学方程式为:CO(g)+FeO(s)=Fe(s)+CO2(g) ΔH= -11kJ/mol;
(3)100mL 0.4mol·L-1 Ba(OH)2的物质的量为0.04mol,向H2SO4溶液中加入100mL 0.4mol·L-1 Ba(OH)2溶液反应涉及的离子方程式有Ba2+(aq)+SO42-(aq)=BaSO4(s),H+(aq)+OH(aq)=H2O(l),100mL 0.4mol·L-1HCl的物质的量为0.04mol,反应涉及的离子方程式为H+(aq)+OH(aq)=H2O(l),根据放出的热量为2.2kJ,可知H+(aq)+OH(aq)=H2O(l) ΔH= -![]() = -55kJmol-1,设Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH= -Q kJ·mol-1,则0.04Q+0.08mol×55kJ·mol-1=5.12kJ,解之得Q=18,所以Na2SO4溶液与BaCl2溶液反应的热化学方程式为Ba2+(aq)+SO42- (aq)=BaSO4(s) ΔH= -18 kJ·mol-1。
= -55kJmol-1,设Ba2+(aq)+SO42-(aq)=BaSO4(s) ΔH= -Q kJ·mol-1,则0.04Q+0.08mol×55kJ·mol-1=5.12kJ,解之得Q=18,所以Na2SO4溶液与BaCl2溶液反应的热化学方程式为Ba2+(aq)+SO42- (aq)=BaSO4(s) ΔH= -18 kJ·mol-1。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。

(1)镍铬钢就是抗腐蚀性能强的新型材料。
①基态Ni原子的电子排布式为________________,铬元素在周期表中____区。
②Ni能与CO形成正四面体形的配合物Ni(CO)4,1 mol Ni(CO)4中含有________ mol σ键。
③NiO的晶体结构如图甲所示,其中离子坐标参数 A 为(0,0,0),B为(1,1,0),则C离子坐标参数为____。
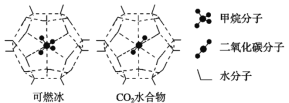
(2)海洋底部有储量丰富的可燃冰,一定条件下,CH4、CO2都能与H2O形成笼状结构(如下图所示)的水合物晶体,其相关参数见下表。CH4与H2O形成的水合物晶体俗称“可燃冰”。
参数 分子 | 分子直径/nm | 分子与H2O的结合能 E/kJ·mol-1 |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | 29.91 |
①“可燃冰”中分子间存在的2种作用力是_____________________。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想。已知如图中笼状结构的空腔直径为0.586 nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________________________________。
(3)①CH4和CO2所含的三种元素电负性从小到大的顺序为_______________
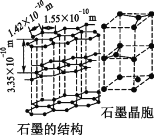
②碳的另一种同素异形体——石墨,其晶体结构如图所示,则石墨晶胞含碳原子个数为____个.已知石墨的密度为ρ g·cm—3,C—C键长为r cm,阿伏加德罗常数的值为NA,计算石墨晶体的层间距为__________cm。