ΧβΡΩΡΎ»ί
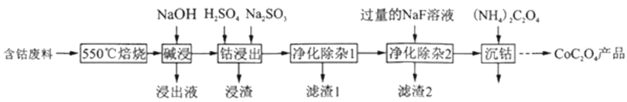
ΓΨΧβΡΩΓΩ≤ίΥανή «÷ΤΉς―θΜ·νήΚΆΫπ τνήΒΡ‘≠ΝœΓΘ“Μ÷÷άϊ”ΟΚ§νήΖœΝœ(÷ς“Σ≥…Ζ÷ΈΣCo2O3,Κ§…ΌΝΩFe2O3ΓΔAl2O3ΓΔCaOΓΔMgOΓΔΧΦΦΑ”–ΜζΈοΒ»)÷Τ»ΓCoC2O4ΒΡΙΛ“’Νς≥Χ»γΆΦ
(1)ΓΑ550Γφ±Κ…’Γ±ΒΡΡΩΒΡ «___ΘΜ
(2)ΓΑΫΰ≥ω“ΚΓ±ΒΡ÷ς“Σ≥…Ζ÷ «___ΘΜ
(3)ΓΑνήΫΰ≥ωΓ±Ιΐ≥Χ÷–Co3+ΉΣΜ·ΈΣCo2+Θ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ___ΘΜ
(4)ΓΑΨΜΜ·≥ΐ‘”1Γ±Ιΐ≥Χ÷–,œ»‘Ύ4050ΓφΦ”»κH2O2,ΤδΉς”Ο «___(”ΟάκΉ”ΖΫ≥Χ Ϋ±μ Ψ);‘Ό…ΐΈ¬÷Ν8085Γφ,Φ”»κNa2CO3»ή“ΚΘ§ΒςpH÷Ν4.5Θ§ΓΑ¬Υ‘ϋ1Γ±÷ς“Σ≥…Ζ÷ΒΡ «___.
(5)ΓΑΨΜΜ·≥ΐ‘”2Γ±Ω…ΫΪΗΤΓΔΟΨάκΉ”ΉΣΜ·ΈΣ≥ΝΒμΙΐ¬Υ≥ΐ»Ξ,»τΥυΒΟ¬Υ“Κ÷–c(Ca2+)=1.0ΓΝl05mol/L,‘ρ¬Υ“Κ÷–c(Mg2+)ΈΣ___[“―÷ΣKsp(MgF2)=7.35ΓΝ1011ΓΔKsp(CaF2)=1.05ΓΝ1010.]
(6)ΈΣ≤βΕ®÷ΤΒΟ―υΤΖΒΡ¥ΩΕ»,œ÷≥Τ»Γ1.00g―υΤΖ,ΫΪΤδ”Ο Β± ‘ΦΝΉΣΜ·,ΒΟΒΫ≤ίΥαοß[(NH4)2C2O4]»ή“Κ,‘Ό”ΟΙΐΝΩœΓΝρΥαΥαΜ·,”Ο0.1000mol/LKMnO4»ή“ΚΒΈΕ®,¥οΒΫΒΈΕ®÷’Βψ ±,Ι≤”Ο»ΞKMnO4»ή“Κ26.00mLΘ§‘ρ≤ίΥανή―υΤΖΒΡ¥ΩΕ»ΈΣ___.(±ΘΝτΝΫΈΜ–Γ ΐ)
ΓΨ¥πΑΗΓΩ≥ΐ»ΞΧΦΚΆ”–ΜζΈο NaAlO2 2Co3++![]() +H2O=2Co2++
+H2O=2Co2++![]() +2H+ 2Fe2++2H++H2O2=2Fe3++2H2O Fe(OH)3 7.0ΓΝ10-6mol/L 95.55%Θ°
+2H+ 2Fe2++2H++H2O2=2Fe3++2H2O Fe(OH)3 7.0ΓΝ10-6mol/L 95.55%Θ°
ΓΨΫβΈωΓΩ
ΗυΨίΝς≥ΧΖ÷ΈωΩ…÷ΣΘ§άϊ”ΟΚ§νήΖœΝœ(÷ς“Σ≥…Ζ÷ΈΣCo2O3Θ§Κ§…ΌΝΩFe2O3ΓΔAl2O3ΓΔCaOΓΔMgOΓΔΧΦΦΑ”–ΜζΈοΒ»)÷Τ»ΓCoC2O4Θ§–η“ΣΫΪΧΦΦΑ”–ΜζΈο‘Ύ550Γφλ―…’≥ΐ»ΞΘ§άϊ”ΟNaOHΫΪAl2O3»ήΫβΉΣΜ·ΈΣNaAlO2Ϋχ»κΫΰ≥ω“ΚΘΜάϊ”ΟΜΙ‘≠ΦΝNa2SO3ΫΪCo3+ΜΙ‘≠ΈΣCo2+Θ§Ά§ ±“≤ΜαΫΪFe3+ΜΙ‘≠ΈΣFe2+ΘΜ‘ΎΓΑΨΜΜ·≥ΐ‘”1Γ±Ιΐ≥Χ÷–Θ§–ηΦ”»κ―θΜ·ΦΝΘ§Ά§ ±ΒςΫΎpHΘ§ΫΪFe2+ΉΣΜ·ΈΣFe3+Θ§ΫχΕχΉΣΜ·ΈΣFe(OH)3≥ΝΒμΘΜ»ΜΚσΦ”»κΙΐΝΩΒΡNaF»ή“ΚΘ§ΫΪMg2+ΓΔCa2+ΉΣΜ·ΈΣMgF2ΓΔCaF2≥ΝΒμ≥ΐ»ΞΘΜΉνΚσΦ”»κ(NH4)2C2O4»ή“ΚΘ§ΫΪCo2+ΉΣΜ·ΈΣCoC2O4Θ§Ψί¥ΥΖ÷ΈωΫβ¥πΓΘ
(1)ΧΦΦΑ”–ΜζΈοΨΏ”–Ω…»Φ–‘Θ§Κ§νήΖœΝœ÷–ΒΡΧΦΦΑ”–ΜζΈο‘Ύ550Γφ±Κ…’ ±Ω…“‘…ζ≥…Εΰ―θΜ·ΧΦΒ»±Μ≥ΐ»ΞΘ§Ι ¥πΑΗΈΣΘΚ≥ΐ»ΞΧΦΚΆ”–ΜζΈοΘΜ
(2)Ης÷÷―θΜ·Έο÷–Θ§÷Μ”–Al2O3»ή”ΎNaOH»ή“ΚΘ§ΖΔ…ζΖ¥”ΠAl2O3+2NaOHΘΫ2NaAlO2+H2OΘ§Υυ“‘ΓΑΫΰ≥ω“ΚΓ±ΒΡ÷ς“Σ≥…Ζ÷ «NaAlO2Θ§Ι ¥πΑΗΈΣΘΚNaAlO2ΘΜ
(3)ΓΑνήΫΰ≥ωΓ±Ιΐ≥Χ÷–Co3+ΉΣΜ·ΈΣCo2+Θ§Ά§ ±Na2SO3ΉΣΜ·ΈΣNa2SO4Θ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2Co3++SO32-+H2O=2Co2++SO42-+2H+ΓΘ¥πΑΗΈΣΘΚ2Co3++SO32-+H2O=2Co2++SO42-+2H+ΘΜ
(4)ΓΑΨΜΜ·≥ΐ‘”1Γ±Ιΐ≥Χ÷–Θ§–ηΦ”»κ―θΜ·ΦΝΘ§Ά§ ±ΒςΫΎpHΘ§ΫΪFe2+ΉΣΜ·ΈΣFe3+Θ§ΫχΕχΉΣΜ·ΈΣFe(OH)3≥ΝΒμΓΘΥυ“‘Θ§‘Ύ40ΓΪ50ΓφΦ”»κH2O2»ή“ΚΘ§ΤδΡΩΒΡ «2Fe2++2H++H2O2=2Fe3++2H2OΘΜ‘Ό…ΐΈ¬÷Ν80ΓΪ85ΓφΘ§Φ”»κNa2CO3»ή“ΚΘ§ΒςpH÷Ν5Θ§ ΙΧζάκΉ”ΉΣΜ·ΈΣ«β―θΜ·Χζ≥ΝΒμΘ§Υυ“‘ΓΑ¬Υ‘ϋIΓ±ΒΡ÷ς“Σ≥…Ζ÷ «Fe(OH)3ΓΘ¥πΑΗΈΣΘΚ2Fe2++2H++H2O2=2Fe3++2H2OΘΜFe(OH)3ΘΜ
(5)ΗυΨίKsp(CaF2) =1.05ΓΝ10-10Θ§»τΥυΒΟ¬Υ“Κ÷–c(Ca2+)=1.0ΓΝl0-5mol /LΘ§‘ρc(F-)=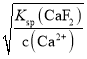 =
=![]() mol /LΘ§‘ρc(Mg2+)=
mol /LΘ§‘ρc(Mg2+)=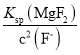 =
=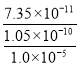 =7.0ΓΝ10-6mol/LΘ§Ι ¥πΑΗΈΣ7.0ΓΝ10-6mol/LΘΜ
=7.0ΓΝ10-6mol/LΘ§Ι ¥πΑΗΈΣ7.0ΓΝ10-6mol/LΘΜ
(6)…η≤ίΥανήΒΡ÷ ΝΩΈΣxΘ§ΗυΨίΖΫ≥Χ ΫΘΚ5H2C2O4+2MnO4-+6H+=2Mn2++10CO2Γϋ+8H2OΘ§≤ίΥαΗυ ΊΚψΩ…ΒΟΘΚ5CoC2O4~5(NH4)2C2O4~5H2C2O4~2MnO4-Θ§‘ρn(CoC2O4)=n(H2C2O4)=![]() ΓΝ0.1000mol/LΓΝ0.026L=0.0065molΘ§ΗΟ≤ζΤΖΒΡ¥ΩΕ»ΈΣ
ΓΝ0.1000mol/LΓΝ0.026L=0.0065molΘ§ΗΟ≤ζΤΖΒΡ¥ΩΕ»ΈΣ![]() =95.55%ΓΘ¥πΑΗΈΣΘΚ95.55%ΓΘ
=95.55%ΓΘ¥πΑΗΈΣΘΚ95.55%ΓΘ

 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ –Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
–Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗΓΨΧβΡΩΓΩάϊ”Ο»γΆΦΥυ ΨΉΑ÷Ο≤βΕ®÷–ΚΆ»»ΒΡ Β―ι≤Ϋ÷η»γœ¬ΘΚ
ΔΌ”ΟΝΩΆ≤ΝΩ»Γ50 mL 0.50 molΓΛLΘ≠1―ΈΥαΒΙ»κ–Γ…’±≠÷–Θ§≤β≥ω―ΈΥαΈ¬Ε»ΘΜ
ΔΎ”ΟΝμ“ΜΝΩΆ≤ΝΩ»Γ50 mL 0.55 molΓΛLΘ≠1 NaOH»ή“ΚΘ§≤Δ”ΟΆ§“ΜΈ¬Ε»ΦΤ≤β≥ωΤδΈ¬Ε»ΘΜ
ΔέΫΪNaOH»ή“ΚΒΙ»κ–Γ…’±≠÷–Θ§…ηΖ® Ι÷°ΜλΚœΨυ‘»Θ§≤βΒΟΜλΚœ“ΚΉνΗΏΈ¬Ε»ΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ

Θ®1Θ©ΗΟΆΦ÷–”–ΝΫ¥ΠΈ¥Μ≠≥ωΘ§ΥϋΟ« «______ΓΔ__________ΓΘ
Θ®2Θ©ΈΣ ≤Ο¥Υυ”ΟNaOH»ή“Κ“Σ…‘ΙΐΝΩ_________________ΓΘ
Θ®3Θ©ΒΙ»κNaOH»ή“ΚΒΡ’ΐ»Ζ≤ΌΉς «_______________________ΓΘ
Θ®4Θ©œ÷ΫΪ“ΜΕ®ΝΩΒΡœΓ«β―θΜ·ΡΤ»ή“ΚΓΔœΓ«β―θΜ·ΗΤ»ή“ΚΓΔœΓΑ±Υ°Ζ÷±πΚΆ1 L 1 molΓΛLΘ≠1ΒΡœΓ―ΈΥα«ΓΚΟΆξ»ΪΖ¥”ΠΘ§ΤδΖ¥”Π»»Ζ÷±πΈΣΠΛH1ΓΔΠΛH2ΓΔΠΛH3Θ§‘ρΠΛH1ΓΔΠΛH2ΓΔΠΛH3ΒΡ¥σ–ΓΙΊœΒΈΣ______ΓΘ
Θ®5Θ©ΦΌ…η―ΈΥαΚΆ«β―θΜ·ΡΤ»ή“ΚΒΡΟήΕ»ΕΦ «1 gΓΛcmΘ≠3Θ§”÷÷Σ÷–ΚΆΖ¥”ΠΚσ…ζ≥…»ή“ΚΒΡ±»»»»ίcΘΫ4.18 JΓΛgΘ≠1ΓΛΓφΘ≠1ΓΘΈΣΝΥΦΤΥψ÷–ΚΆ»»Θ§Ρ≥―ß…ζ Β―ιΦ«¬Φ ΐΨί»γœ¬ΘΚ
Β―ι –ρΚ≈ | Τπ ΦΈ¬Ε»t1/ Γφ | ÷’÷ΙΈ¬Ε»t2/ Γφ | |
―ΈΥα | «β―θΜ·ΡΤ»ή“Κ | ΜλΚœ»ή“Κ | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
“άΨίΗΟ―ß…ζΒΡ Β―ι ΐΨίΦΤΥψΘ§ΗΟ Β―ι≤βΒΟΒΡ÷–ΚΆ»»ΠΛHΘΫ______(ΫαΙϊ±ΘΝτ“ΜΈΜ–Γ ΐ)ΓΘ
Θ®6Θ©____(ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±)”ΟBa(OH)2»ή“ΚΚΆΝρΥα¥ζΧφ«β―θΜ·ΡΤ»ή“ΚΚΆ―ΈΥαΘ§άμ”… «______ΓΘ