题目内容
(15分)甲醇(CH3OH)是用来制备汽油添加剂和许多普通塑料的原料,低温液相合成甲醇的方法如下。
反应原理:2H2+ CO→CH3OH;反应条件:以三乙二醇二甲醚作为溶剂,以Raney-Ni和CH3ONa为催化剂。
(1)氢碳比[γ =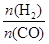 ]:当γ=2时,甲醇的选择性[λ =
]:当γ=2时,甲醇的选择性[λ =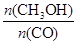 ]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。
]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。
(2)干燥除水:为防止CH3ONa的水解,必须干燥除水,下表是不同干燥方法时对CO转化率的影响。
从实验设计完整性思考,请补充实验⑤中的干燥方法。
(3)反应温度:下图是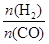 = 2时甲醇合成过程中压力和温度随时间变化的图像。
= 2时甲醇合成过程中压力和温度随时间变化的图像。
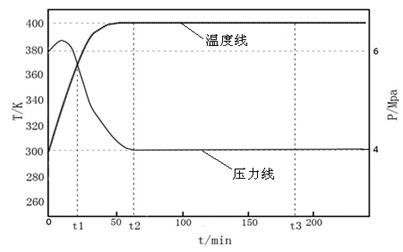
在反应CO(g)+2H2(g)→CH3OH(g) △H中,△H 0(填“>”或“<”);0~t2时间段内,随反应的进行体系的压力先增大后减小,原因是 ;能判断该反应基本结束的时刻为 ;若t3时刻,测得平衡后CO的转化率为75%,若起始反应时的CO的物质的量为a mol,假设反应容器的体积为1L,则t3时的平衡常数的值为 。
(4)催化剂:在保持其它条件不变,只改变催化剂的用量,分别在1L恒容密闭容器中反应,测定10min时的CO转化率。下图是Raney-Ni为0.05g时,CO转化率与时间关系图,请画出Raney-Ni为1g时,CO转化率与时间变化图。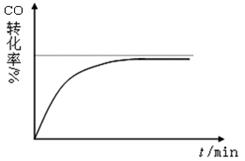
反应原理:2H2+ CO→CH3OH;反应条件:以三乙二醇二甲醚作为溶剂,以Raney-Ni和CH3ONa为催化剂。
(1)氢碳比[γ =
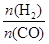 ]:当γ=2时,甲醇的选择性[λ =
]:当γ=2时,甲醇的选择性[λ =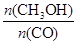 ]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。
]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。(2)干燥除水:为防止CH3ONa的水解,必须干燥除水,下表是不同干燥方法时对CO转化率的影响。
| 序号 | 干燥方法 | CO转化率/% |
| ① | 不处理 | 40.2 |
| ② | 无水乙醇洗 | 56.3 |
| ③ | 以四氢呋喃洗 | 62.4 |
| ④ | 无水乙醇洗并真空干燥 | 70.1 |
| ⑤ | | 77.2 |
(3)反应温度:下图是
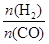 = 2时甲醇合成过程中压力和温度随时间变化的图像。
= 2时甲醇合成过程中压力和温度随时间变化的图像。
在反应CO(g)+2H2(g)→CH3OH(g) △H中,△H 0(填“>”或“<”);0~t2时间段内,随反应的进行体系的压力先增大后减小,原因是 ;能判断该反应基本结束的时刻为 ;若t3时刻,测得平衡后CO的转化率为75%,若起始反应时的CO的物质的量为a mol,假设反应容器的体积为1L,则t3时的平衡常数的值为 。
(4)催化剂:在保持其它条件不变,只改变催化剂的用量,分别在1L恒容密闭容器中反应,测定10min时的CO转化率。下图是Raney-Ni为0.05g时,CO转化率与时间关系图,请画出Raney-Ni为1g时,CO转化率与时间变化图。

(1)3H2+ CO→CH4+H2O (2分) (2)以四氢呋喃洗并真空干燥 (2分)
(3)< (2分) 反应开始时因温度升高,压力增大;随着反应的进行,气体物质的量减少,压力降低(2分) t2 (2分)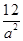 (2分)
(2分)
(4) (3分,若画出的曲线与原来曲线相同,也给分)
(3分,若画出的曲线与原来曲线相同,也给分)
(3)< (2分) 反应开始时因温度升高,压力增大;随着反应的进行,气体物质的量减少,压力降低(2分) t2 (2分)
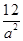 (2分)
(2分)(4)
 (3分,若画出的曲线与原来曲线相同,也给分)
(3分,若画出的曲线与原来曲线相同,也给分)试题分析:(1)根据质量守恒定律,生成CH4外还应该生成水,故化学方程式为3H2+ CO→CH4+H2O。(2)为使实验具有可比性,以四氢呋喃洗涤时也应该真空干燥。(3)从图像可看出,随着反应的进行,温度升高,说明反应放热,即△H<0;反应为放热反应,开始时温度升高,则压强增大;随着反应的进行,气体减少,则压强降低;t2时,温度和压强都不再发生变化,说明反应已基本结束;CO的起始浓度为amol/L,平衡浓度为(1-75%)amol/L,H2的平衡浓度为2×(1-75%)amol/L,CH4OH的平衡浓度为0.75amol/L,故平衡常数为K =
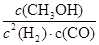 =
= 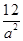 L-2·mol-2。(4)题目本意是增加催化剂的量,反应速率加快,即到达平衡的时间缩短,但不改变平衡状态。
L-2·mol-2。(4)题目本意是增加催化剂的量,反应速率加快,即到达平衡的时间缩短,但不改变平衡状态。
练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案
相关题目
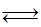 2HI(g) ΔH =" -14.9" kJ/mol,实验时有关数据如下表:
2HI(g) ΔH =" -14.9" kJ/mol,实验时有关数据如下表:
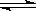 3C(g)+D(g),以下不能说明已达平衡状态的是
3C(g)+D(g),以下不能说明已达平衡状态的是 Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是
Ni(CO)4(g),已知该反应平衡常数与温度的关系下表,下列说法正确的是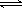 2NH3(g) ΔH=-92.4 kJ·mol
2NH3(g) ΔH=-92.4 kJ·mol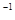 ):
): C(g)+D(g) ΔH<0。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 molA和1 mol B,在Ⅱ中充入1 mol C和1 mol D,在Ⅲ中充入2 mol A和2 mol B,500℃条件下开始反应。达到平衡时,下列说法正确的是
C(g)+D(g) ΔH<0。现有三个相同的2 L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1 molA和1 mol B,在Ⅱ中充入1 mol C和1 mol D,在Ⅲ中充入2 mol A和2 mol B,500℃条件下开始反应。达到平衡时,下列说法正确的是  2Z(g);ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( )
2Z(g);ΔH<0。为了使平衡向生成Z的方向移动,应选择的条件是( ) 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是 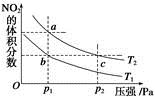
 2HI(g)达平衡, 加压后混合气体颜色变深
2HI(g)达平衡, 加压后混合气体颜色变深