题目内容
下列变化不能用勒夏特列原理解释的是( )
| A.工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 |
B.已知反应 H2(g)+ I2(g) 2HI(g)达平衡, 加压后混合气体颜色变深 2HI(g)达平衡, 加压后混合气体颜色变深 |
| C.红棕色的NO2加压后颜色先变深再变浅 |
| D.实验室用排饱和食盐水的方法收集氯气 |
B
试题分析:A.在工业上制取硫酸的关键反应是2SO2+O2
 2SO3。由于该反应是可能反应。若使用过量的氧气,即增大了氧气的浓度,关键平衡移动原理:增大反应物的浓度,平衡正向移动,可以使更多的SO2转化为SO3。因此二氧化硫的转化率提高。正确。B. 已知反应 H2(g)+ I2(g)
2SO3。由于该反应是可能反应。若使用过量的氧气,即增大了氧气的浓度,关键平衡移动原理:增大反应物的浓度,平衡正向移动,可以使更多的SO2转化为SO3。因此二氧化硫的转化率提高。正确。B. 已知反应 H2(g)+ I2(g) 2HI(g)达平衡,由于该反应是反应前后气体体积相等的可能反应。加压平衡不发生移动。但是由于加压后单位体积内的I2的物质的量增大,所以浓度增大,混合气体颜色变深。正确。C.在密闭容器内NO2存在化学平衡:2NO2(g)
2HI(g)达平衡,由于该反应是反应前后气体体积相等的可能反应。加压平衡不发生移动。但是由于加压后单位体积内的I2的物质的量增大,所以浓度增大,混合气体颜色变深。正确。C.在密闭容器内NO2存在化学平衡:2NO2(g) N2O4(g)NO2是红棕色的气体,N2O4是无色气体。加压后单位体积内NO2增多,所以气体的颜色先变深。由于该反应的正反应是气体体积减小的反应。增大压强,化学平衡向正反应方向移动,所以气体的颜色又逐渐变浅。但是颜色比加压前深。正确。D.氯气在水中存在化学平衡:Cl2+H2O
N2O4(g)NO2是红棕色的气体,N2O4是无色气体。加压后单位体积内NO2增多,所以气体的颜色先变深。由于该反应的正反应是气体体积减小的反应。增大压强,化学平衡向正反应方向移动,所以气体的颜色又逐渐变浅。但是颜色比加压前深。正确。D.氯气在水中存在化学平衡:Cl2+H2O H++Cl-+HclO。若水中存在NaCl。则食盐电离产生的Cl-会使c(Cl-)增大。根据平衡移动原理:增大生成物的浓度,平衡向逆反应方向移动。因此可以减小氯气在水中的溶解和反应而引起的消耗。故实验室用排饱和食盐水的方法收集氯气。正确。
H++Cl-+HclO。若水中存在NaCl。则食盐电离产生的Cl-会使c(Cl-)增大。根据平衡移动原理:增大生成物的浓度,平衡向逆反应方向移动。因此可以减小氯气在水中的溶解和反应而引起的消耗。故实验室用排饱和食盐水的方法收集氯气。正确。
练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
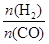 ]:当γ=2时,甲醇的选择性[λ =
]:当γ=2时,甲醇的选择性[λ =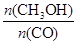 ]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。
]达99.8%以上;当γ>2时,可能产生副产物CH4,写出相应反应的化学方程式 。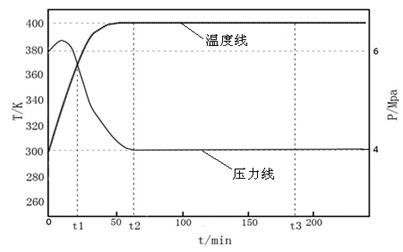
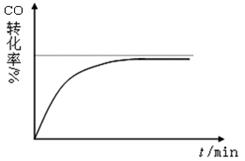
 2HBr(g),已知加入1 mol H2和2 mol Br2达到平衡后,生成了a mol HBr。在相同条件下,若起始时加入的H2、Br2、HBr分别为x mol、y mol、z mol(均不为0)且保持平衡时,各组分百分含量都不变。以下推断中一定正确的是
2HBr(g),已知加入1 mol H2和2 mol Br2达到平衡后,生成了a mol HBr。在相同条件下,若起始时加入的H2、Br2、HBr分别为x mol、y mol、z mol(均不为0)且保持平衡时,各组分百分含量都不变。以下推断中一定正确的是 2NH3(g)(正反应为放热反应),下列说法中正确的是( )
2NH3(g)(正反应为放热反应),下列说法中正确的是( ) 4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
4C(s)+2D(g),反应一段时间后达到平衡,测得生成1.6 mol C,则下列说法正确的是
 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是( )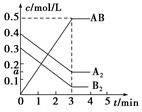
 2Z(g)+Q,在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n与反应时间t的关系如下图所示。下列判断正确的是( )
2Z(g)+Q,在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n与反应时间t的关系如下图所示。下列判断正确的是( )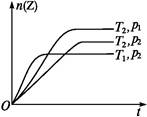
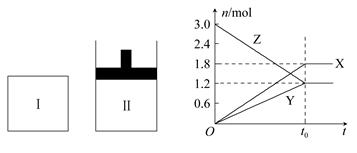
 3Z
3Z