题目内容
4. 由软锰矿制备高锰酸钾的主要反应如下:
由软锰矿制备高锰酸钾的主要反应如下:Ⅰ.熔融氧化 3MnO2+KClO3+6KOH$\frac{\underline{\;熔融\;}}{\;}$3K2MnO4+KCl+3H2O
Ⅱ.加酸歧化法3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
或电解法 2K2MnO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2KMnO4+2KOH+H2↑
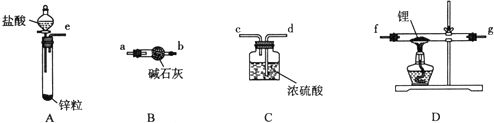
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和cd(填字母).
a.蒸发皿 b.瓷坩埚 c.铁坩埚 d.泥三角
(2)加酸时不宜用盐酸的原因是盐酸具有还原性,会被氧化,降低产品的量;
(3)写出采用电解法时的阳极反应式MnO42--e-═MnO4-;与加酸歧化相比,电解法的明显优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率;
(4)草酸钠滴定法分析高锰酸钾纯度步骤如下:
①称取0.80g 左右的高锰酸钾产品,配成100mL溶液.
②准确称取0.2014g左右已烘干的Na2C2O4,置于锥形瓶中,加入少量蒸馏水使其溶解,再加入少量硫酸酸化.
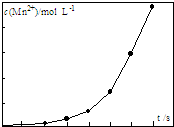
③将瓶中溶液加热到75~80℃,趁热用①中配制的高锰酸钾溶液滴定至终点.记录消耗高锰酸钾溶液的体积,计算得出产品纯度.滴定过程中反应的离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O;将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如图,其原因可能为生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快;加热温度大于90℃,部分草酸发生分解,会导致测得产品纯度偏高.(填“偏高”、“偏低”或“无影响”).
分析 (1)熔融固体物质需要再坩埚内加热,加热熔融物含有碱性KOH应用铁坩埚、铁棒、坩埚钳、泥三角、酒精灯;
(2)盐酸具有还原性,会被氧化,降低产品的量;
(3)阳极是锰酸根离子失电子生成高锰酸根离子,与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率;
(4)③根据高锰酸钾与草酸钠发生氧化还原反应书写反应的离子方程式;反应中Mn2+浓度发生显著变化,应是反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好,加热温度大于90℃,部分草酸发生分解,消耗高锰酸钾溶液的体积减少,会导致测得产品纯度偏高;
解答 解:(1)熔融固体物质需要再坩埚内加热,加热熔融物含有碱性KOH应用铁坩埚、铁棒、坩埚钳、泥三角、酒精灯,故答案为:c d;
(2)盐酸具有还原性,会被氧化,降低产品的量,故不宜用盐酸,
故答案为:盐酸具有还原性,会被氧化,降低产品的量;
(3)采用电解法时的阳极反应式,是锰酸根离子失电子生成高锰酸根离子,电极反应:MnO42--e-═MnO4-;与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率,
故答案为:MnO42--e-═MnO4-;K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率;
(4)③高锰酸钾与草酸钠发生氧化还原反应,反应的离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,反应中Mn2+浓度发生显著变化,应是反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好,加热温度大于90℃,部分草酸发生分解,消耗高锰酸钾溶液的体积减少,会导致测得产品纯度偏高,
故答案为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O;生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快;偏高.
点评 本题考查氧化还原反应离子方程式的书写、氧化还原反应滴定等,难度中等,注意把握实验的原理,需要学生具备一定的理论分析能力和计算解决问题的能力.

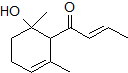 ,可用于制作香水.有关该化合物的下列说法正确的是( )
,可用于制作香水.有关该化合物的下列说法正确的是( )| A. | 分子式为C12H20O2 | B. | 该化合物可使酸性KMnO4溶液褪色 | ||
| C. | 该化合物可与NaOH溶液发生反应 | D. | 1 mol该化合物可与2 mol Br2加成 |
| A. | 2:1 | B. | 1:3 | C. | 2:3 | D. | 1:2 |
| A. | ③④ | B. | ①②④ | C. | ①②③④ | D. | ②④ |
| A. | 不容易腐蚀 | B. | 比较硬 | C. | 强度大 | D. | 密度小 |
| A. | H2、O2 | B. | SO2、H2S | C. | NO、O2 | D. | HCl、NH3 |