题目内容
5.在2L的容器里有某反应物4mol,反应进行2秒后,该反应物还剩3.2mol,则该反应的平均速率为( )(mol•L-1•s-1)| A. | 0.1 | B. | 0.2 | C. | 0.4 | D. | 0.8 |
分析 进行2s后,该反应中△n=(4-3.2)mol=0.8mol,根据v=$\frac{\frac{△n}{V}}{△t}$计算平均反应速率,据此分析解答.
解答 解:进行2s后,该反应中△n=(4-3.2)mol=0.8mol,v=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.8mol}{2L}}{2s}$=0.2mol•L-1•s-1,故选B.
点评 本题考查化学反应速率有关计算,明确公式中各个物理量的关系即可解答,题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
15.将pH值为8的NaOH溶液与pH值为10的NaOH溶液等体积混合后,溶液的H+ 浓度最接近于( )
| A. | $\frac{1}{2}$(10-8+10-10)mol•L-1 | B. | (10-8+10-10)mol•L-1 | ||
| C. | (1×10-14-5×10-5)mol•L-1 | D. | 2×10-10mo1•L-1 |
16.要使有机物HO COOH转化为HO
COOH转化为HO COONa,可选用的试剂是( )
COONa,可选用的试剂是( )
 COOH转化为HO
COOH转化为HO COONa,可选用的试剂是( )
COONa,可选用的试剂是( )| A. | Na | B. | Na2CO3 | C. | NaHCO3 | D. | NaOH |
20.下列物质中和铜不发生反应的是( )
| A. | 稀硝酸 | B. | 浓硝酸 | C. | 浓硫酸 | D. | 稀硫酸 |
10.下列实验装置图正确的是( )
| A. | 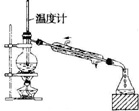 蒸馏石油 | B. | 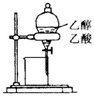 除去乙醇中的乙酸 | ||
| C. | 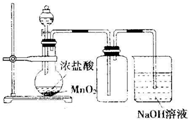 实验室制氯气 | D. | 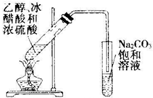 实验室制乙酸乙酯 |
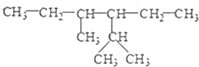 的系统命名为:2,4-二甲基-3-乙基乙烷
的系统命名为:2,4-二甲基-3-乙基乙烷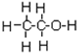 ,乙烯的电子式为
,乙烯的电子式为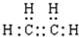
 <
<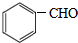
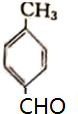
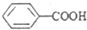 >CH3COOH(提示:类比酚与醇的酸性)
>CH3COOH(提示:类比酚与醇的酸性)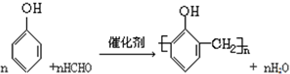
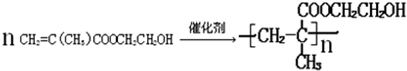 .
.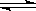 N204(无色) △H<0。将一定量的NO2充入注射器中后封口,右下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是( )
N204(无色) △H<0。将一定量的NO2充入注射器中后封口,右下图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小)。下列说法正确的是( )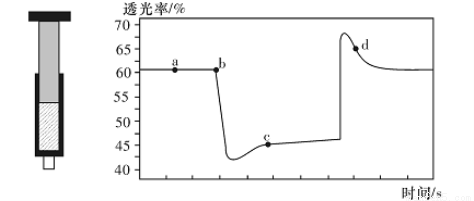
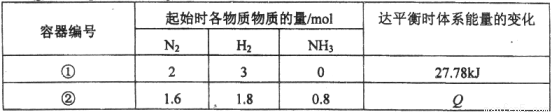
 H2(g)
H2(g) 2NH3(g) △H= -92.6 kJ / mol。测得数据如下表:
2NH3(g) △H= -92.6 kJ / mol。测得数据如下表: