题目内容
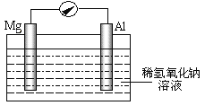
【题目】利用LiOH和钴氧化物可制备锂离子电池正极材料。可用电解LiCl溶液制备LiOH,装置如图所示。下列说法正确的是
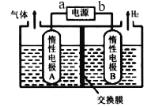
A.惰性电极B是阳极
B.电流流向为a→A→B→b
C.该电解池用的交换膜是阴离子交换膜
D.阳极发生的电极反应方程式:4OH- - 4e-=O2↑+2H2O
【答案】B
【解析】
电解LiCl溶液制备LiOH,由图可知,右侧生成氢气,则右侧溶液中应为水电离出的氢离子放电,同时生成氢气和氢氧根离子,B为阴极,阳极为Cl-放电生成氯气,为防止生成的LiOH与氯气反应,应用阳离子交换膜,Li+由A经过阳离子交换膜向B移动,在B中得到LiOH,阴阳两电极区电解液分别为LiOH和LiCl溶液,据此根据电解池的工作原理来解答。
A. 由以上分析知,惰性电极B是阴极,故A错误;
B. B为阴极,A为阳极,则a为电源的正极,b为电源的负极,则电流流向为a→A→B→b,故B正确;
C. 由以上分析知,该电解池用的交换膜是阳离子交换膜,故C错误;
D. 阳极为Cl-放电生成氯气,电极反应方程式为:2Cl--2e-=Cl2↑,故D错误;
故选B。

练习册系列答案
相关题目