题目内容
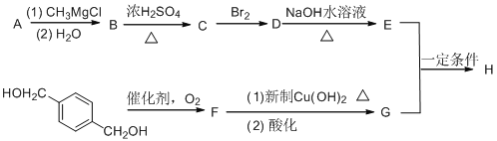
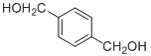
【题目】通过对淀粉水解产物的综合利用,可以获得多种有机物。它们之间的转化关系如下(含有相同官能团的有机物通常具有相似的化学性质):
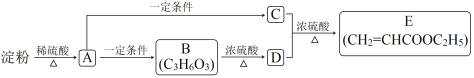
已知B能与Na2CO3反应,B的催化氧化产物不能发生银镜反应,且1mol B与足量金属钠反应产生1mol H2。
请回答:
(1)D中所含官能团名称是___________。(2)B的结构简式是_______________。
(3)C+D→E的化学方程式是____________。
(4)下列说法正确的是_________。
A.将一小粒钠投入C中,钠始终浮在液面上缓慢放出气泡,同时得到能使酚酞试液变红的物质
B.在一定条件下,D和E都能通过加聚反应生成高聚物
C.共mg A和B的混合物在氧气中完全燃烧,消耗22.4m/30 L氧气
D.B在浓硫酸作用下反应可能生成六元环状化合物
【答案】碳碳双键 羧基 ![]() CH2=CH-COOH+C2H5OH
CH2=CH-COOH+C2H5OH ![]() H2O +CH2=CH-COOC2H5 B D
H2O +CH2=CH-COOC2H5 B D
【解析】
淀粉在稀硫酸的作用下水解生成葡萄糖;已知B能与Na2CO3反应,则含有羧基,B的催化氧化产物不能发生银镜反应,且1mol B与足量金属钠反应产生1mol H2,则羟基在中间碳原子上则B的结构简式为:![]() ;B生成D时为醇羟基的消去反应,生成CH2=CH-COOH;A一定条件下反应生成乙醇,则C为乙醇;C与D发生酯化反应生成E和水;
;B生成D时为醇羟基的消去反应,生成CH2=CH-COOH;A一定条件下反应生成乙醇,则C为乙醇;C与D发生酯化反应生成E和水;
(1)D的结构简式为:CH2=CH-COOH,含有的官能团为碳碳双键、羧基;
(2)根据分析可知,B的结构简式为:![]() ;
;
(3)C与D发生酯化反应生成E和水,反应方程式为:CH2=CH-COOH+C2H5OH ![]() CH2=CH-COOC2H5 +H2O ;
CH2=CH-COOC2H5 +H2O ;
(4)A.C的结构简式为:CH2=CH-COOH,密度比水大,加入Na,迅速产生气泡,反应生成氢气和CH2=CH-COONa,A错误;
B.反应物D、E中均含有碳碳双键,都能通过加聚反应生成高聚物,B正确;
C. 共m gA和B的混合物在氧气中完全燃烧,消耗标况下的22.4m/30L氧气,C错误;
D. B的结构简式为:![]() ,两个B可以发生酯化反应生成
,两个B可以发生酯化反应生成 ,D正确;
,D正确;
答案为BD

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】t℃时,在一个体积为2L密闭容器中加入反应物A、B,发生如下反应:A(s)+2B(g)![]() 3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
3C(g)。反应过程中的部分数据如下表所示,下列说法正确的是
物质 | 起始 | 2分钟 | 4分钟 | 6分钟 |
A | 2 mol | 1.2 mol | ||
B | 6 mol | 3.0 mol | ||
C | 0 mol | x mol | 4.5 mol |
A. 前2分钟内,A的反应速率为0.2molL-1min-1
B. 表中x的值为3.6
C. 4分钟时,反应达到平衡状态,此时正、逆反应的速率都为0
D. 升高温度,正、逆反应的速率都会增大