题目内容
【题目】某强酸性溶液X中可能含有Fe2+、Al3+、![]() 、
、![]() 、
、![]() 、
、![]() 、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如图,下列说法正确的是( )
、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如图,下列说法正确的是( )
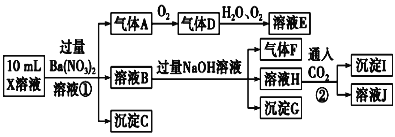
A.气体A是NO2
B.X溶液中肯定存在Fe2+、Al3+、![]() 、
、![]()
C.溶液E和气体F不能发生化学反应
D.X溶液中不能确定的离子是Al3+和Cl-
【答案】D
【解析】
强酸性溶液,一定不含![]() 、
、![]() ;加入硝酸钡,有白色沉淀生成,说明一定含有
;加入硝酸钡,有白色沉淀生成,说明一定含有![]() ;加入硝酸钡,有气体生成,说明一定含有还原性离子Fe2+,生成的气体A是NO,D是NO2,E是HNO3;溶液B一定含有Fe3+、Ba2+,加入氢氧化钠生成沉淀Fe(OH)3,同时生成气体F,F是NH3,说明原溶液含有
;加入硝酸钡,有气体生成,说明一定含有还原性离子Fe2+,生成的气体A是NO,D是NO2,E是HNO3;溶液B一定含有Fe3+、Ba2+,加入氢氧化钠生成沉淀Fe(OH)3,同时生成气体F,F是NH3,说明原溶液含有![]() ;溶液H一定含有Ba2+,通入二氧化碳气体,生成沉淀I,则I是碳酸钡或碳酸钡和Al(OH)3的混合物,则原溶液可能含有Al3+。
;溶液H一定含有Ba2+,通入二氧化碳气体,生成沉淀I,则I是碳酸钡或碳酸钡和Al(OH)3的混合物,则原溶液可能含有Al3+。
根据分析,A. 气体A是NO,故A错误;
B. X溶液中可能含有Al3+,故B错误;
C. 溶液E是硝酸、气体F是氨气,发生反应生成硝酸铵,故C错误;
D. X溶液中一定有Fe2+、![]() 、
、![]() ,一定不含
,一定不含![]() 、
、![]() ,不能确定的离子是Al3+和Cl-,故D正确。
,不能确定的离子是Al3+和Cl-,故D正确。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】滴定实验是化学学科中重要的定量实验。请回答下列问题:
(1)酸碱中和滴定——用浓度为0.1000mol·L-1的标准盐酸滴定未知浓度的NaOH溶液,表格中记录了实验数据:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.50 | 20.40 |
第二次 | 20.00 | 3.00 | 23.00 |
第三次 | 20.00 | 4.00 | 24.10 |
①下列操作造成测定结果偏高的是________(填选项字母)
A.滴定终点读数时,俯视滴定管刻度,其他操作正确。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,盛装标准液的滴定管尖嘴有气泡,滴定后气泡消失
②该NaOH溶液的物质的量浓度为_____________mol/L。(小数点后保留四位有效数字)
(2)氧化还原滴定——取一定量的草酸(H2C2O4)溶液置于锥形瓶中,加入适量稀硫酸,用标准酸性高锰酸钾溶液滴定。滴定时KMnO4溶液应装在______________(填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是_________________________________。
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是______(填选项字母)。
难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaClB.NaBrC.NaCND.Na2CrO4