题目内容
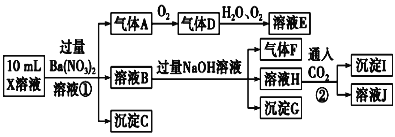
【题目】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献.联合制碱法的主要过程如图所示(部分物质己略去)

(1)①~③所涉及的操作方法中,包含过滤的是________(填序号)
(2)根据上图,写出①中发生反应的化学方程式:________
(3)煅烧![]() 固体的化学方程式是_____________
固体的化学方程式是_____________
(4)下列说法中,正确的是________(填字母)
a.![]() 可循环使用
可循环使用
b.副产物![]() 可用作肥料
可用作肥料
c.溶液B中一定含有![]() 、
、![]() 、
、![]()
【答案】① ③ ![]()
![]() a b c
a b c
【解析】
根据图示过程分析可知,向饱和食盐水中先通入氨气,再通入CO2气体,发生反应:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,将NaHCO3过滤出来,加热发生分解反应![]() ,得到纯碱Na2CO3,滤液中加入NaCl固体,会析出NH4Cl晶体;
,得到纯碱Na2CO3,滤液中加入NaCl固体,会析出NH4Cl晶体;
(1)根据上述分析可知,①~③所涉及的操作方法中,包含过滤的是①和③;
(2)过程①为向饱和食盐水中先通入氨气,再通入CO2气体,发生反应生成NaHCO3和NH4Cl,反应的化学方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(3)NaHCO3受热分解产生Na2CO3、H2O和CO2,反应的化学方程式为![]() ;
;
(4)a.开始通入二氧化碳反应,最后碳酸氢钠受热分解生成的CO2可循环使用,a正确;
b.副产物NH4Cl是氮肥,可用作植物生长所需的肥料,b正确;
c.溶液B中主要是氯化钠、氯化铵饱和溶液,一定含有Na+、![]() 、Cl-,c正确;
、Cl-,c正确;
故合理选项是abc。

【题目】下列实验结论与实验操作及现象不相符的一组是( )
选项 | 实验操作及现象 | 实验结论 |
A | 向某酸雨样品中加入Ba(OH)2溶液,有白色沉淀生成 | 酸雨试样中一定含SO42- |
B | 向KI-淀粉溶液中滴入氯水,溶液变成蓝色 | I-的还原性强于Cl- |
C | 将Ba(OH)2·8H2O和NH4Cl晶体在小烧杯中混合搅拌,用手触摸烧杯外壁感觉变凉 | Ba(OH)2·8H2O与NH4Cl的反应是吸热反应 |
D | 向某盐溶液中加入NaOH溶液,加热,用湿润的红色石蕊试纸放在试管口,试纸变蓝 | 该盐溶液中含有NH4+ |
A.AB.BC.CD.D